
题目列表(包括答案和解析)
A.N2、P4、CCl4 B.CCl4、CO2、SiCl4
C.XeF6、H2O2、PCl3 D.PCl5、BF3、BeCl2
请按要求回答下列问题:
(1)画出E的离子结构示意图____________,写出由A和C组成的含有非极性键的化合物的电子式:____________。
(2)由上述元素组成的化合物中属于极性键构成的非极性分子的是____________(只要求写出两种,用化学式表示)。
(3)由C与E形成的化合物高温时与B反应生成两种化合物,请写出该反应的化学方程式:________________________。
(4)写出上述元素形成的化合物中一种可溶性的正盐与另一种强酸反应的离子方程式:________________________。
(5)上述元素形成的化合物中通常能污染空气的是________________________(至少写出两种)。某一种可污染空气的化合物与强氧化剂单质常温下反应生成两种化合物,该反应的化学方程式为:_____________________________________________________________________。
原子序数依次增大的A、B、C、D、E五种短周期元素。B、C、D位于同一周期相邻位置,B和D的原子最外层电子数之比为2∶3;B、C、D分别与A形成的化合物分子中都含有10个电子;E的原子结构示意图中从内到外各层的电子数之比为1∶4∶1。则下列叙述中正确的是
A.B和D形成的某种化合物能与E的单质在一定条件下发生置换反应
B.实验室制备A和C两种元素形成的化合物发生的反应属于氧化还原反应
C.由B、D原子或A、B原子构成的分子都是非极性分子
D.由A、B、C、D四种元素组成的化合物中不可能含有离子键
 短周期元素A、B、C、D原子序数依次增大,且C元素最高价氧化物对应的水化物,能电离出电子数相等的阴、阳离子.A、C位于同一主族,A为非金属元素,B的最外层电子数是次外层的3倍,B、C的最外层电子数之和与D的最外层电子数相等.E单质是生活中常见金属,其制品在潮湿空气中易被腐蚀或损坏.
短周期元素A、B、C、D原子序数依次增大,且C元素最高价氧化物对应的水化物,能电离出电子数相等的阴、阳离子.A、C位于同一主族,A为非金属元素,B的最外层电子数是次外层的3倍,B、C的最外层电子数之和与D的最外层电子数相等.E单质是生活中常见金属,其制品在潮湿空气中易被腐蚀或损坏.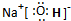
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com