(1)南京“青奥会”已进入倒计时,体育场馆和城市交通建设日臻完善.
①体育场馆建设需大量建筑材料.下列材料不属于硅酸盐材料的是
a
a
(填字母)
a、石灰石 b、水泥 c、玻璃
②轨道交通建设需要大量金属材料.下列金属材料最容易发生腐蚀的是
b
b
(填字母)
a、铝合金 b、钢铁 c、纯铜
③“塑胶”跑道是由聚氨酯橡胶等材料建成.聚氨酯橡胶属于
c
c
(填字母)
a、金属材料 b、无机非金属材料 c、有机高分子材料
(2)“青奥会”期间,要保障运动员的营养与健康.
①及时补充体能是运动员取得优秀成绩的基本保证.六大营养素中能在人体内氧化供能的有糖类、
油脂
油脂
和
蛋白质
蛋白质
.
②运动员还要吸收合理的维生素,在维生素C的结构为
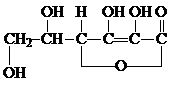
,其分子式为
C6H8O6
C6H8O6
;在氯化铁溶液中加入维生素C后,溶液由黄色转变为浅绿色,说明维生素C具有较强的
还原性
还原性
性.
③服用违禁药物不仅妨碍体育竞技的公平、公正,也有害运动员的身心健康.在阿司匹林、青霉素、麻黄素、小苏打等常用药物中,参赛选手不可服用的是
麻黄素
麻黄素
.
(3)“绿水蓝天”工程为运动员提供优良环境,向世界展示古都南京的美好形象.
①PM2.5指悬浮于大气中的直径≤2.5μm(微米)的颗粒物,大量PM2.5会造成灰霾天气,危害人体健康.燃煤气化有助于控制PM2.5的含量,写出焦炭与水蒸气反应的化学方程式
.
②汽车必须使用无铅汽油,其原因是
防治铅污染
防治铅污染
.
③含铬元素的废水必须治理达标.某兴趣小组处理含Cr
2O
72-的废水的方法是用(NH
4)
2Fe(SO
4)
2将其还原为Cr
3+,再用氨水将Cr
3+转变成难溶的Cr(OH)
3.写出用氨水将Cr
3+转变成难溶的Cr(OH)
3的离子方程式
Cr3++3NH3?H2O=Cr(OH)3↓+3NH4+
Cr3++3NH3?H2O=Cr(OH)3↓+3NH4+
;该方案处理后的废水中因含有大量
N(或氮)
N(或氮)
元素,导致水体富营养化.

![]() 发生加成反应生成烃W,W不能通过化学反应使溴水褪色,但能使酸性高锰酸钾溶液褪色;在另外的条件下,1molW还能与
发生加成反应生成烃W,W不能通过化学反应使溴水褪色,但能使酸性高锰酸钾溶液褪色;在另外的条件下,1molW还能与![]() 发生加成反应生成含乙基的环状化合物。
发生加成反应生成含乙基的环状化合物。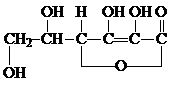 ,其分子式为
,其分子式为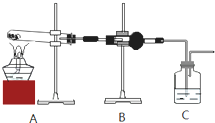
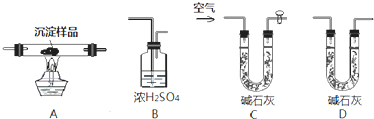
 氮的氧化物和SO2是常见的化工原料,但也是大气的主要污染物.综合治理其污染是化学家研究的主要内容.根据题意完成下列各题:
氮的氧化物和SO2是常见的化工原料,但也是大气的主要污染物.综合治理其污染是化学家研究的主要内容.根据题意完成下列各题: