(2011?翠屏区模拟)理论上,SO
2能发生类似CO
2与澄清石灰水作用的反应,但在通常实验中,将SO
2通入澄清石灰水却没有看到类似CO
2那样先浑浊后澄清的现象.针对这一问题,研究性学习小组开展了探究性实验.
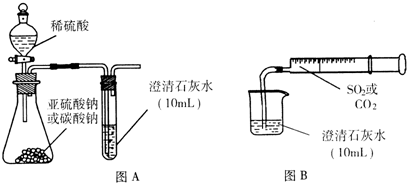
I.用图A所示的装置来分别做CO
2、SO
2与澄清石灰水的反应实验,结果通入CO
2可看到先浑浊后澄清的现象,但通入SO
2没看到浑浊现象.
Ⅱ.用图B的装置,将气体收集在注射器里,缓慢地将气体一个气泡一个气泡地通入澄清石灰水中,无论CO
2还是SO
2都能看到“先变浑再澄清”的现象.当以相同速率分别通入CO
2或SO
2,通入SO
2产生现象明显比通入CO
2产生现象快.
回答下列问题:
(1)通过上述I、Ⅱ实验,可以确定,将足量SO
2缓慢通入澄清石灰水,依次发生的反应有:(用离子方程式表示)
SO2+Ca2++2OH-═CaSO3↓+H2O
SO2+Ca2++2OH-═CaSO3↓+H2O
;
CaSO3+H2O+SO2=Ca2++2HSO3-
CaSO3+H2O+SO2=Ca2++2HSO3-
.
(2)实验I中,通入SO
2不能出现浑浊的原因可能是:
澄清的石灰水比较少,通入二氧化硫较快较多,两者反应时直接生成了易溶于水的酸式盐,而看不到沉淀
澄清的石灰水比较少,通入二氧化硫较快较多,两者反应时直接生成了易溶于水的酸式盐,而看不到沉淀
.
(3)实验Ⅱ中,同速率分别通入CO
2或SO
2,SO
2产生现象比CO
2快的相关因素有
①③⑤⑥
①③⑤⑥
.
①SO
2在水中溶解度比CO
2大.
②相同状态下,SO
2的密度比CO
2的密度大.
③亚硫酸酸性比碳酸强,在同温度、同体积的溶液中,l mol亚硫酸电离产生的H
+离子浓度大于l mol碳酸电离产生的H
+离子浓度.
④SO
2有毒和刺激性气味,CO
2无毒和无刺激性气味.
⑤相同条件下,1mol SO
2与足量石灰水反应生成CaSO
3的速率大于1mol CO
2与足量石灰水反应生成CaCO
3的速率.
⑥相同条件下,1molCaSO
3被1mol SO
2(形成的H
+离子)溶解形成可溶性Ca(HSO
3)
2的速率大于1molCaCO
3被1molCO
2(形成的H
+离子)溶解形成可溶性Ca(HCO
3)
2的速率.

