
题目列表(包括答案和解析)
| A、适量CO2通入氯化钙溶液中:CaCl2+CO2+H2O=CaCO3↓+2HCl | ||||
| B、碳酸氢镁和过量石灰水反应:Mg(HCO3)2+Ca(OH)2=MgCO3↓+CaCO3↓+H2O | ||||
C、把氯水放在阳光下:2HClO
| ||||
| D、向碳酸氢钙溶液中加入少量NaOH溶液:Ca(HCO3)2+2NaOH=CaCO3↓+Na2CO3+2H2O |



| ||


| O | 2- 3 |
| O | - 3 |
| O | 2- 3 |
| O | - 3 |
| O | 2- 3 |
| O | - 3 |
| O | 2- 3 |
| O | - 3 |
洪灾过后,饮用水的消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一。漂白粉是常用的消毒剂。根据所学知识,回答下列问题:
(1)工业上将氯气通入石灰乳制取漂白粉,化学反应方程式为____________________。
(2)漂白粉溶于水后,受空气中的CO2作用,即产生有漂白、杀菌作用的次氯酸,化学反应方程式为___________________________________ 。
(3)制取漂白粉的氯气可通过电解饱和食盐水得到。在电解食盐水之前,需要提纯食盐水。为了除去粗盐中的Ca2+、Mg2+、SO42-及泥沙,可将粗盐溶于水,然后进行下列五项操作,正确的操作顺序是 。
①过滤 ②加过量的NaOH溶液 ③加适量的盐酸
④加过量的Na2CO3溶液 ⑤加过量的BaCl2溶液
A、①④②⑤③ B、④①②⑤③ C、②⑤④①③ D、⑤②④③①
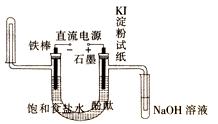
(4) 极滴入酚酞先变红色(填阴或阳),石墨棒的一端能使湿润的淀粉碘化钾试纸 。
(5)假如电解饱和食盐水制取氯气,氯气制取漂白粉过程中没有任何损耗,得到715g次氯酸钙的同时,理论上需要消耗NaCl的物质的量为多少? (4分)
洪灾过后,饮用水的消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一。漂白粉是常用的消毒剂。根据所学知识,回答下列问题:
(1)工业上将氯气通入石灰乳制取漂白粉,化学反应方程式为____________________。
(2)漂白粉溶于水后,受空气中的CO2作用,即产生有漂白、杀菌作用的次氯酸,化学反应方程式为 _______ ____________________________ 。
____________________________ 。
(3)制取漂白粉的氯气可通过电解饱和食盐水得到。在电解食盐水之前,需要提纯食盐水。为了除去粗盐中的Ca2+、Mg2+、SO42-及泥沙,可将粗盐溶于水,然后进行下列五项操作,正确的操作顺序是 。
①过滤 ②加过量的NaOH溶液 ③加适量的盐酸
④加过量的Na2CO3溶液 ⑤加过量的BaCl2溶液
| A.①④②⑤③ | B.④①②⑤③ | C.②⑤④①③ | D.⑤②④③① |
 g次氯酸钙的同时,理论上需要消耗NaCl的物质的量为多少? (4分)
g次氯酸钙的同时,理论上需要消耗NaCl的物质的量为多少? (4分)湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com