
题目列表(包括答案和解析)
 已知NO2和N2O4可以相互转化:2NO2(g)?N2O4(g)△H<0.现将一定量NO2和N2O4的混合气体通入一定体积为2L的恒温密闭玻璃容器中,反应物浓度随时间变化关系如图所示.
已知NO2和N2O4可以相互转化:2NO2(g)?N2O4(g)△H<0.现将一定量NO2和N2O4的混合气体通入一定体积为2L的恒温密闭玻璃容器中,反应物浓度随时间变化关系如图所示.| 10 |
| 9 |
| 10 |
| 9 |
用NA表示阿伏加德罗常数的值.下列叙述中不正确的是
A.分子总数为NA的SO2和CO2混合气体中含有的原子数为3NA
B.28 g乙烯和环丁烷(C4H8)的混合气体中含有的氢原子数为4NA
C.常温常压下,92 g的NO2和N2O4混合气体含有的氧原子数为4 NA
D.标准状况下,22.4L氧气与足量铁粉充分反应,转移的电子数为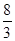 NA
NA
|
设NA表示阿伏加德罗常数值,下列说法正确的是 | |
| [ ] | |
A. |
1 mol Cl2与足量Fe反应,转移的电子数为3NA |
B. |
1.5 mol NO2与足量H2O反应,转移的电子数为1.5NA |
C. |
常温常压下,46 g NO2和N2O4混合气体含有的原子数为3NA |
D. |
含HCL 1.0 mol的浓盐酸与足量MnO2反应,生成Cl2的分子数为0.25NA |
若NA表示阿伏加德罗常数,下列说法正确的是
A.Na2O和Na2O2的混合物共1mol,阴离子数目在NA~2NA 之间
B.常温常压下,92 g NO2和N2O4的混合气体中含有的分子数目为2NA
C.一定条件下,密闭容器充入1molN2和3molH2充分反应,转移电子的数目为6NA
D.FeCl3溶液中,若Fe3+数目为NA,则Cl—数目大于3NA
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com