
题目列表(包括答案和解析)
(1)镁与稀硫酸反应的离子方程式为_____________________________________________。
(2)铝与氧化铁发生铝热反应的化学方程式为_____________________________________。
(3)在潮湿的空气里,钢铁表面有一层水膜,很容易发生电化学腐蚀,其中正极的电极反应为_____________________________________________________________________。
(4)在海洋工程上,通常用铝合金(AlZnCd)保护海底钢铁设施,其原理如下图所示:
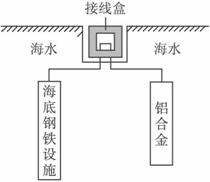
其中负极发生的电极反应为______________________________________________________;
在实际应用中,用铝合金而不选用纯铝。纯铝不能很好地起到保护作用,其原因是______。
(5)将11.9 gMg-Al-Fe组成的合金溶于足量NaOH溶液中,合金质量减少
将7.8 g过氧化钠与足量的水充分反应,所得溶液的体积为100 mL。试计算:(1)生成氧气的体积(标准状况)。(2)反应后所得溶液中溶质的物质的量浓度。(上述计算均要求写出计算过程)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com