
题目列表(包括答案和解析)
在实验室中拟用氧化铜、稀硫酸和锌来制取纯净的铜并验证铜的有关性质,甲、乙两位同学分别设计了如下实验方案。
甲:①CuO溶于适量稀硫酸中;
②在①的溶液中加入适量锌,反应一段时间后,过滤、烘干,即得纯净的铜。
乙:①锌与稀硫酸反应得氢气;
②将氢气通过氧化铜中并加热,充分反应一段时间后即得纯净的铜。请填空:
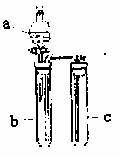
(1)丙同学发现上述两方案制得的铜都含有杂质,则甲、乙方案制得的铜所含杂质分别是 和 。
(2)现欲用乙方案制得纯净的铜,你认为应怎样补充完善方案,简述操作
步骤 。
(3)现用制得的纯净的铜进行如下实验,如右图在c中加适量NaOH溶液,b中放适量制得的铜,由分液漏斗a向b中加入2 mL稀硝酸,则b中反应的离子方程式是 ,实验中观察到的现象是 。
在实验室中拟用氧化铜、稀硫酸和锌制取纯净的铜,甲、乙两同学分别设计了如下实验方案。
甲:①将CuO溶于适量的稀硫酸中;
②在①的溶液中加入适量的锌,充分反应后,过滤、烘干,即得纯净的铜。
乙:①锌与稀硫酸反应得氢气;
②将氢气通入氧化铜中并加热,充分反应后即得纯净的铜。
问:若要制得相同质量的纯铜,甲乙所耗用的锌和稀硫酸是否相同?为什么?
。
丙同学认为上述两种方案所制得的铜都难以保证铜的纯度,应对上述两种方案加以完善。你是否同意丙同学的看法?为什么?你认为应该怎样完善实验方案?
。
如图是实验室用启普发生器制取氢气,用以还原氧化铜制取较纯净的Cu的装置图.

(1)实验前,锌粒由________处加入;稀硫酸由________处加入.
(2)检验装置气密性的方法是________.
(3)用氢气还原氧化铜的操作包括:①打开旋塞;②加热试管;③检验氢气纯度;④关闭旋塞;⑤撤除酒精灯;⑥冷却.其操作顺序是(只填写编号)________,
若步骤⑤与⑥操作搞错了,实验结果将会________.
检验反应后是否残余氧化铜的方法是________.
(4)不能用浓硫酸跟锌起反应制取氢气的理由是________.
(8分)请用相关知识回答下列问题:
(1)用纯净的碳酸钙与稀盐酸反应制取二氧化碳气体,实验过程测得的CO2气体体积随时间变化如右图所示。
①________段化学反应速率最快,_______段收集的二氧化碳气体最多。
②除加入蒸馏水外,当加入下列物质中的 (填序号)时,则能够减缓上述反应的速率。
A.醋酸钠溶液 B.碳酸钙粉末 C.稀硫酸 D.浓盐酸
(2)原电池是一种能量装置。
①下列在理论上可用来设计原电池的反应是 (填序号)。
A.NaOH +HCl==NaCl+H2O B.2FeCl3+Cu=2FeCl2+CuCl2
C.CuSO4 +2NaOH== Cu(OH)2+NaSO4 D.C2H6O +3O2==3H2O+2CO2
②实验室中用锌片与硫酸反应制取氢气时,向反应溶液中滴加几滴CuSO4溶液,可以发现产生氢气速率明显加快,其原因是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com