
题目列表(包括答案和解析)
镁、铝、铁是重要的金属,在工业生产中用途广泛。
(1)镁与稀硫酸反应的离子方程式为 ;
(2)铝与氧化铁发生铝热反应的化学方程式为 ;
(3)在潮湿的空气里,钢铁表面有一层水膜,很容易发生电化学腐蚀。其中正极的电极反应为 ;
(4)在海洋工程上,通常用铝合金(Al―Zn―Cd)保护海底钢铁设施,其原理如图所示:
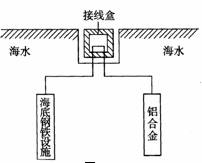
其中负极发生的电极反应为 ;
在实际应用中,用铝合金而不选用纯铝。纯铝不能很好地起到保护作用,其原因是 。(5)将11.9g Mg―Al―Fe组成的合金溶于足量NaOH溶液中,合金质量减少2.7g。另取等质量的合金溶于过量的稀硝酸中,生成6.72L(标准状况)NO,向反应后的溶液中加入适量的NaOH溶液恰好使Mg2+、Al3+、Fe3+完全转化为沉淀,则沉淀的质量为 g
镁、铝都是较活泼的金属,在一定条件下能与氧、氮等起反应.镁铝合金粉可用作烟火材料.
(a)取此合金粉与足量的稀硫酸反应,在大气压为101325 Pa,温度为25℃时,在水面上收集到气体的体积为0.5052 L.
(b)另取等量的此合金粉在氧气中燃烧,将燃烧产物用足量的稀硫酸处理,将不溶物用水洗净烘干,称重为0.3399克.
(c)再取等量的此合金粉使之在空气中燃烧,将燃烧产物用足量的稀氢氧化钠溶液处理,将溶液滤去,残渣先用氢氧化钠溶液洗涤,然后用水洗净,再将残渣在高温下灼烧至恒重,得0.7090克.(25℃时,饱和水蒸气压为3167 Pa,R=8.314 kPa·L·mol-1·K-1).
(1)求产生H2的物质的量;
(2)求在氧气中燃烧时生成MgO的质量;
(3)写出(c)中的各步化学反应方程式;
(4)求在空气中燃烧时生成Al2O3的质量;
(5)求合金粉中Al的百分含量.
| |||||||||||||||||||||||
(13分)合金已成为飞机制造、化工生产等行业的重要材料。研究性学习小组的同学,为测定某含镁3%~5%的铝镁合金(不含其它元素)中镁的质量分数,设计下列两种不同实验方案进行探究。填写下列空白。
〖实验方案一〗将铝镁合金与足量NaOH溶液反应,测定剩余固体质量。实验中发生反应的化学方程式是 。
〖实验步骤〗
(1)称取5.4 g铝镁合金粉末样品,溶于V mL 2.0 moI·L-1NaOH溶液中,充分反应。则NaOH溶液的体积V ≥ 。
(2)过滤、洗涤、干燥、称量固体。该步骤中若未洗涤固体,测得镁的质量分数将 (填“偏高”、“偏低”或“无影响”)。
〖实验方案二〗将铝镁合金与足量稀硫酸溶液反应,测定生成气体在通常状况(约20℃,1.01×105Pa)的体积。
〖问题讨论〗(3)同学们拟选用下列实验装置完成实验:
①你认为最简易的装置其连接顺序是(填接口字母,可不填满):
A接( )( )接( )( )接( )
②实验开始时,先打开分液漏斗上口的玻璃塞,再轻轻打开其活塞,一会儿后稀硫酸也不能顺利滴入锥形瓶。请你帮助分析原因。 。
③实验结束时,在读取测量实验中生成氢气的体积时,你认为合理的是 。
A.待实验装置冷却后再读数
B.上下移动量筒F,使其中液面与广口瓶中液面相平
C.上下移动量筒G,使其中液面与广口瓶中液面相平
D.视线与凹液面的最低点水平,读取量筒中水的体积
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com