
题目列表(包括答案和解析)
 已知反应mA(g)+nB(g)?xC(g)+yD(g),A的转化率RA与P、T的关系如图,根据图示可以得出的正确结论是( )
已知反应mA(g)+nB(g)?xC(g)+yD(g),A的转化率RA与P、T的关系如图,根据图示可以得出的正确结论是( )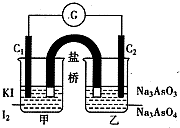 (2012?武汉模拟)已知反应“As
(2012?武汉模拟)已知反应“As| O | 3- 4 |
| O | 3- 3 |
 已知反应X(g)+Y(g)?nZ(g)△H<0,将X和Y 以一定比例混合通入2L密闭容器中进行反应,各物质的浓度随时间的改变如图所示.下列说法正确的是( )
已知反应X(g)+Y(g)?nZ(g)△H<0,将X和Y 以一定比例混合通入2L密闭容器中进行反应,各物质的浓度随时间的改变如图所示.下列说法正确的是( )| A、反应方程式中n=2 | B、该反应的△S>0 | C、10min时,曲线发生变化的原因是增大压强 | D、0~5min内,平均反应速率v(X)=0.04mol?L-1?min-1 |
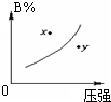 已知反应mA(s)+nB(g)?pC(g)△H<0,在一定温度下达到平衡时B的体积分数(B%)与压强的关系如图所示,下列判断错误的是( )
已知反应mA(s)+nB(g)?pC(g)△H<0,在一定温度下达到平衡时B的体积分数(B%)与压强的关系如图所示,下列判断错误的是( )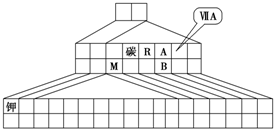 如图是元素周期表的另一种画法--三角形元素周期表的一部分,图上标有第ⅦA族和碳、钾两种元素的位置.
如图是元素周期表的另一种画法--三角形元素周期表的一部分,图上标有第ⅦA族和碳、钾两种元素的位置.
| ||
| ||
| ||
| ||
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com