
题目列表(包括答案和解析)
(1)□KMnO4+□KNO2+□![]() =□MnSO4+□K2SO4+□KNO3+□H2O;
=□MnSO4+□K2SO4+□KNO3+□H2O;
(2)□(NH4)2MoO4+□Zn+□HCl=□MoCl3+□ZnCl2+□NH4Cl+□![]() ;
;
(3)□Na2CrO4+□Na2S+□H2O=□Cr(OH)3↓+□Na2SO4+□![]() 。
。
配平下列化学方程式,将化学计量数和所缺的物质的化学式填入相应的空格内。
(1)□KMnO4+□KNO2+□![]() =□MnSO4+□K2SO4+□KNO3+□H2O;
=□MnSO4+□K2SO4+□KNO3+□H2O;
(2)□(NH4)2MoO4+□Zn+□HCl=□MoCl3+□ZnCl2+□NH4Cl+□![]() ;
;
(3)□Na2CrO4+□Na2S+□H2O=□Cr(OH)3↓+□Na2SO4+□![]() 。
。

| ||
| ||
| 方案 质量 |
方案甲 | 方案乙 |
| U型管+固体 | 硬质玻璃管+固体 | |
| 反应前质量/g | a | c |
| 完全反应后质量/g | b | d |
| 16(d+w-c) |
| c-d |
| 16(d+w-c) |
| c-d |

| 方案 质量 | 方案甲 | 方案乙 |
| U型管+固体 | 硬质玻璃管+固体 | |
| 反应前质量/g | a | c |
| 完全反应后质量/g | b | d |
Ⅰ无水氯化铝是某些有机化学反应中常用的催化剂,它的熔点190℃,但在180℃时已开始升华.它在常温下是一种白色固体,遇水发生剧烈的水解反应,甚至在空气中遇到微量水汽也强烈地发烟.用下列装置制取无水氯化铝:
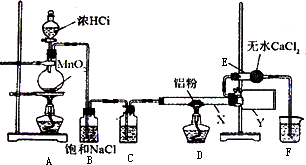
回答以下问题:
(1)装置D中发生的化学反应方程式:________.
(2)仪器X与仪器Y直接相连的意图是:
①收集产物
②________.
(3)能否去掉E装置________原因是________.
(4)实验时应先点燃________处的酒精灯,其作用是________.
Ⅱ.某种胃药中止酸剂为CaCO3.为测定其中CaCO3的含量,某化学小组设计了以下方案(药片中的其他成分与HCl和NaOH溶液均不反应):
用滴定法测定,有以下几步操作:
A.配制0.100 mol/L HCl溶液和0.100 mol/L NaOH溶液
B.取一粒药片(0.100 g),研碎后加入20.0 mL蒸馏水
C.以酚酞为指示剂用0.100 mol/L NaOH溶液滴定,用去NaOH溶液VmL时达到终点
D.用酸式滴定管加入25.00 mL 0.100 mol/L HCl溶液,充分反应
请回答有关问题:
(1)测定过程的正确操作顺序为________(填字母).
(2)经测定,每次消耗NaOH溶液体积的平均值为13.00 mL,则该胃药中CaCO3的质量分数是________.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com