
题目列表(包括答案和解析)
现有五种溶液:NaCl、 K2S 、NaAlO2 、NaHCO3 、BaCl2要求只用一种试剂一次将它们区分开来,这种试剂可以是下列的 ( )
A.稀盐酸 B.稀硫酸 C.氯化钡溶液 D.硝酸银溶液
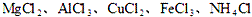 五种溶液,只用一种试剂把它们区别开,这种试剂是
五种溶液,只用一种试剂把它们区别开,这种试剂是 现有![]() 五种溶液,如果只用一种试剂把它们区分开来,这种试剂是
五种溶液,如果只用一种试剂把它们区分开来,这种试剂是
[
]A
.氨水 B.湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com