
题目列表(包括答案和解析)

浓度与反应速率的关系
c(H2)/mol·L-1 | c(Cl2)/mol·L-1 | v/mol·L-1·s-1 |
1.0 | 1.0 | 1.0k |
2.0 | 1.0 | 2.0k |
2.0 | 4.0 | 4.0k |
由此可以推出,m、n的值正确的是( )?
A.m=1,n=1? B.m=![]() ,n=
,n=![]()
C.m=![]() ,n=1 D.m=1,n=
,n=1 D.m=1,n=![]()
①CH3CH2CH3:Ω=0;②(CH3)2CH—:Ω=0;③CH2=CHCH2—:Ω=1; ④![]() :Ω=1;⑤C8H15—:Ω=1;⑥
:Ω=1;⑤C8H15—:Ω=1;⑥![]() :Ω=2;⑦
:Ω=2;⑦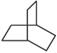 :Ω=2; ⑧CH3C≡CCH2CH=CH2:Ω=3;⑨CH3(CH=CH)3CH3:Ω=3;⑩
:Ω=2; ⑧CH3C≡CCH2CH=CH2:Ω=3;⑨CH3(CH=CH)3CH3:Ω=3;⑩![]() :Ω=4。
:Ω=4。
(1)请写出下列各烃分子的Ω。
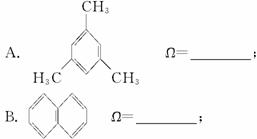
C.立方烷:![]() (正立方体的每个顶点上有一个碳原子,每个碳原子上有一个氢原子) Ω=____________。
(正立方体的每个顶点上有一个碳原子,每个碳原子上有一个氢原子) Ω=____________。
(2)请写出下列烃基的Ω。
D.![]() (2价基团) Ω=_______________;
(2价基团) Ω=_______________;
E.![]() (3价基团) Ω=__________________;
(3价基团) Ω=__________________;
F. ![]() (2价基团) Ω=_________。
(2价基团) Ω=_________。
烷烃可以根据分子里所含_________数目来命名。_________数在10以内的用甲、乙、丙、丁、_________、_________、_________、_________、_________、_________来表示。例如,CH4叫_________,C5H12叫_________。碳原子数在10以上的用数字来表示。例如,C17H36叫_________。前面提到的戊烷的三种异构体,可用“正”“异”“新”来区别,这种命名方法叫习惯命名法。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com