(2011?宣城二模)某校化学兴趣小组为了探究粗铁粒(含有少量金属铜杂质)与某浓度硝酸反应,设计了如下探究活动:
探究一
(1)将粗铁粒投入某浓度硝酸中,某同学观察该实验现象时发现,反应进行一段时间后,反应开始逐渐加快.请分析反应逐渐加快的可能原因
反应放热,一段时间后溶液温度升高,反应速率加快;②由于铁中含杂质铜,反应时形成Fe-Cu微型原电池,加快反应速率
反应放热,一段时间后溶液温度升高,反应速率加快;②由于铁中含杂质铜,反应时形成Fe-Cu微型原电池,加快反应速率
.
(2)另称取粗铁粒10g放入某浓度硝酸中,充分反应后得到溶液X并收集到气体Y.为了探究溶液X中铁元素的价态,同学甲设计如下实验:有药品和仪器:0.1mol?L
-1 KSCN溶液;0.1mol?L
-1 KI溶液;0.2mol?L
-1酸性高锰酸钾溶液;氯水等;试管和滴管
请你设计简单实验,探究上述猜想是否正确,填写下列实验报告:
| 实验步骤 |
现象 |
结论 |
离子方程式 |
| 第一步 |
取2-3mL溶液装于试管,向试管中加入几滴KSCN溶液. |
若溶液变红色,则溶液含有Fe3+;
若无现象,则不含Fe3+ 若溶液变红色,则溶液含有Fe3+;
若无现象,则不含Fe3+ |
Fe3++3SCN-=Fe(SCN)3 Fe3++3SCN-=Fe(SCN)3 |
| 第二步 |
另取少量溶液装于试管,向试管里滴加几滴酸性高锰酸钾溶液 另取少量溶液装于试管,向试管里滴加几滴酸性高锰酸钾溶液 |
若溶液紫色褪去,则溶液含有Fe2+;
若无明显变化,则不含Fe3+. |
5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O 5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O |
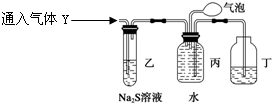
探究二 为了探究气体Y的成分,同学乙设计了如下装置(不考虑NO
2转化为N
2O
4)
(3)装置乙的作用:
验证NO2的存在并除去NO2
验证NO2的存在并除去NO2
.
(4)装置丙收集到满气体后,通过气泡鼓入空气后,有红棕色气体生成,能否确定气体Y中含NO?说明理由.
不能确定,由于NO2与水反应也能生成NO,故不能确定气体Y中含NO
不能确定,由于NO2与水反应也能生成NO,故不能确定气体Y中含NO
.
(5)同学丁为了探究气体Y的组成,将224mL气体Y通入足量的NaOH溶液中,气体被完全吸收,所得溶液再用0.15mol?L
-1酸性KMnO
4溶液滴定,消耗20mL KMnO
4溶液.则气体Y中NO、NO
2的体积比为
1:3
1:3
.(已知2NO
2+2NaOH=NaNO
3+NaNO
2+H
2O和NO
2+NO+2NaOH=2NaNO
2+H
2O)

 (2011?宣城二模)某校化学兴趣小组为了探究粗铁粒(含有少量金属铜杂质)与某浓度硝酸反应,设计了如下探究活动:
(2011?宣城二模)某校化学兴趣小组为了探究粗铁粒(含有少量金属铜杂质)与某浓度硝酸反应,设计了如下探究活动: