
题目列表(包括答案和解析)
某化学课堂上同学们正在进行酸、碱、盐知识的探究,以下是教学片断,请你参与其中并认真填写空格.
【学生实验】将二氧化碳分别通入澄清石灰水和氢氧化钠溶液中,观察到前者变浑浊,后者无明显现象.
【学生板演】澄清石灰水变浑浊的原理 (用化学方程式表示)
【提出问题】二氧化碳通入氢氧化钠溶液中无明显现象,两者是否发生了化学反应?
【猜想假设】猜想①:两者发生了化学反应;猜想②:两者没有发生化学反应
【实验探究】
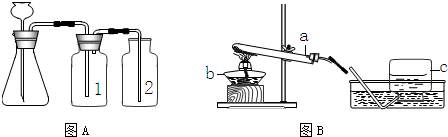
(1)小华设计了如图所示的A、B两个实验.
实验现象:A中软塑料瓶変瘪,B中
(2)小红认为小华的实验是可行的,其共同原理是二氧化碳和氢氧化钠溶液反应,使容器内压强降低.小明同学却对此提出质疑,他认为小华的实验不严谨,其理由是 ,要得到科学严谨的结论,仍利用该装置,补做的对比实验是 .
(3)小宁设计的是通过检验生成物来验证猜想,请帮她填写实验报告.
| 实验步骤 | 实验现象 | 实验结论 |
| 向B实验后的溶液中加入 | | 验证了二氧化碳和氢氧化钠溶液反应 |
一化学兴趣小组对某月饼包装盒中的“脱氧剂”很好奇,他们观察到“脱氧剂”外包装标注的成分为铁粉、活性炭和氯化钠,打开发现灰黑色的固体中还夹杂着少量红棕色粉末.
【资料获悉】铁系“脱氧剂”的作用原理是利用铁能被氧气氧化,从而达到除氧保鲜的目的.
【教师指导】铁被氧气氧化最终产物为红棕色的Fe2O3(其他产物忽略不计).
【探究目的】小组同学欲探究该“脱氧剂”是否已经失效(即单质铁是否已经完全被氧化),并测定各成分的质量分数,设计了以下探究实验.
【实验探究】步骤1:小刚用磁铁接近样品,发现磁铁吸引了部分黑色固体.步骤2:称取10.00g样品与一烧杯中,加足量水充分搅拌溶解后,过滤,将滤渣洗涤、干燥、称得其质量为7.28g.步骤3:按如下装置,将得到的7.28g固体与足量稀硫酸反应,用电子秤称得反应前后总质量差为0.15g.
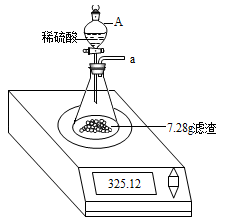
步骤4:将锥形瓶中反应后的液体过滤,并将滤渣洗涤、干燥后,称得其质量为1.20g.
| 说明书 主要成分:碳酸镁 适 应 症:用于缓解胃酸过多引起的胃痛. 用 法:嚼碎后服用 注意事项:胃溃疡患者慎服. |
| 设计方案 | 实验现象 | 结论 |
| 实验一 将一片完整的药片放入试管中,向其中加入5ml 5%的稀盐酸 实验二 将一片药片________后,放入试管中,再加入5ml 5%的稀盐酸 | 实验一比实验二 反应________ (填“快”、“慢”) | 小牛的猜想是合理的 |

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com