
题目列表(包括答案和解析)
![]() 根据硫化氢气体的实验室制法和性质完成下列填空。
根据硫化氢气体的实验室制法和性质完成下列填空。
![]() 若用启普发生器制取硫化氢气体,则制取气体的原料可选用________。
若用启普发生器制取硫化氢气体,则制取气体的原料可选用________。
![]() a.稀硫酸与硫化亚铁 b.稀硝酸与硫化亚铁
a.稀硫酸与硫化亚铁 b.稀硝酸与硫化亚铁
![]() c.稀硫酸与硫化钠 d.稀盐酸与硫化亚铁
c.稀硫酸与硫化钠 d.稀盐酸与硫化亚铁
![]() 现要组装一套可以控制硫化氢气体产生速率的装置,请在下图中选择合适的仪器;
现要组装一套可以控制硫化氢气体产生速率的装置,请在下图中选择合适的仪器;
![]()
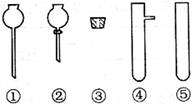 ______________(填编号)。
______________(填编号)。
![]()
![]()
![]()
![]()
![]()
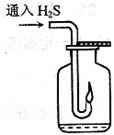
![]() 如右图,在一个充满氧气的集气瓶中加入少量品红稀硫溶液,
如右图,在一个充满氧气的集气瓶中加入少量品红稀硫溶液,
![]() 点燃硫化氢气体。在火焰自动熄灭后,停止通入气体,瓶内可观察到
点燃硫化氢气体。在火焰自动熄灭后,停止通入气体,瓶内可观察到
![]() 的现象是___________________________________________________。
的现象是___________________________________________________。
![]() 在上述集气瓶中继续通入硫化氢气体,振荡,发生反应的化学方程式为:
在上述集气瓶中继续通入硫化氢气体,振荡,发生反应的化学方程式为:
![]() ______________________________________________________________
______________________________________________________________
![]() 反应过程中,溶液的pH______(填“变大”、“变小”或“不变”)。
反应过程中,溶液的pH______(填“变大”、“变小”或“不变”)。
![]() 点燃不纯的硫化氢气体可能会发生爆炸,为了防止意外,可连接一个安全装置。下图的装置能起到此作用的是___________。
点燃不纯的硫化氢气体可能会发生爆炸,为了防止意外,可连接一个安全装置。下图的装置能起到此作用的是___________。
![]()
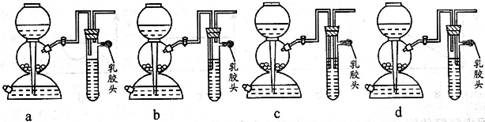
![]() 已知硫化氢气体在空气中的体积分数为4.3%~45.5%时会发生爆炸。当硫化氢气体在空气中的体积分数为30%时,其爆炸产物是______________________。
已知硫化氢气体在空气中的体积分数为4.3%~45.5%时会发生爆炸。当硫化氢气体在空气中的体积分数为30%时,其爆炸产物是______________________。
(12分)在实验室里可用右图所示装置制取氯酸钾、次氯酸钠和探究氯水的性质。
图中:①为氯气发生装置;②的试管里盛有15 mL 30% KOH溶液,并置于水浴中;③的试管里盛有15 mL 8% NaOH溶液,并置于冰水浴中;④的试管里加有紫色石蕊试液;⑤为尾气吸收装置。请填写下列空白:

(1)装置①是氯气发生装置,蒸馏烧瓶中盛放MnO2固体,其反应的化学方程式为 ▲ 。
(2)如果实验室中MnO2用完了,则下列物质可能可以用来代替MnO2制Cl2的是: ▲ 。A.NaBiO3 B.FeCl3 C.PbO2 D.Na2O2
已知氧化性强弱顺序为:NaBiO3>PbO2>MnO2>Na2O2>FeCl3
 (3)比较制取氯酸钾和次氯酸钠的条件,二者的差异是
(3)比较制取氯酸钾和次氯酸钠的条件,二者的差异是
① ▲ ; ② ▲ 。
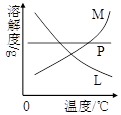
(4)反应完毕经冷却后,②的试管中有大量晶体析出。右图中符合该晶体溶解度曲线的是 ▲ (填写编号字母);从②的试管中分离出该晶体的方法是 ▲ (填写实验操作名称)。
(5)根据④的试管里紫色石蕊试液的颜色变化可否证明氯气的强氧化性 ▲ 。
为什么? ▲ 。
(6)若②的试管溶液中不但有KClO3生成还有KClO生成,且二者的物质的量之比为1∶2,则该反应中氧化剂和还原剂的物质的量之比为: ▲ 。
(12分)在实验室里可用右图所示装置制取氯酸钾、次氯酸钠和探究氯水的性质。
图中:①为氯气发生装置;②的试管里盛有15 mL 30% KOH溶液,并置于水浴中;③的试管里盛有15 mL 8% NaOH溶液,并置于冰水浴中;④的试管里加有紫色石蕊试液;⑤为尾气吸收装置。请填写下列空白:
(1)装置①是氯气发生装置,蒸馏烧瓶中盛放MnO2固体,其反应的化学方程式为 ▲ 。
(2)如果实验室中MnO2用完了,则下列物质可能可以用来代替MnO2制Cl2的是: ▲ 。A.NaBiO3 B.FeCl3 C.PbO2 D.Na2O2
已知氧化性强弱顺序为:NaBiO3>PbO2>MnO2>Na2O2>FeCl3
 (3)比较制取氯酸钾和次氯酸钠的条件,二者的差异是
(3)比较制取氯酸钾和次氯酸钠的条件,二者的差异是
① ▲ ; ② ▲ 。
(4)反应完毕经冷却后,②的试管中有大量晶体析出。右图中符合该晶体溶解度曲线的是 ▲ (填写编号字母);从②的试管中分离出该晶体的方法是 ▲ (填写实验操作名称)。
(5)根据④的试管里紫色石蕊试液的颜色变化可否证明氯气的强氧化性 ▲ 。
为什么? ▲ 。
(6)若②的试管溶液中不但有KClO3生成还有KClO生成,且二者的物质的量之比为1∶2,则该反应中氧化剂和还原剂的物质的量之比为: ▲ 。
(12分)在实验室里可用右图所示装置制取氯酸钾、次氯酸钠和探究氯水的性质。
图中:①为氯气发生装置;②的试管里盛有15 mL 30% KOH溶液,并置于水浴中;③的试管里盛有15 mL 8% NaOH溶液,并置于冰水浴中;④的试管里加有紫色石蕊试液;⑤为尾气吸收装置。请填写下列空白: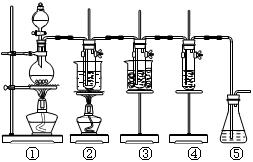
(1)装置①是氯气发生装置,蒸馏烧瓶中盛放MnO2固体,其反应的化学方程式为 ▲ 。
(2)如果实验室中MnO2用完了,则下列物质可能可以用来代替MnO2制Cl2的是: ▲ 。
| A.NaBiO3 | B.FeCl3 | C.PbO2 | D.Na2O2 |
 (3)比较制取氯酸钾和次氯酸钠的条件,二者的差异是
(3)比较制取氯酸钾和次氯酸钠的条件,二者的差异是铝及铝合金经过阳极氧化,铝表面能生成几十微米的较厚的氧化铝膜。

Ⅰ.某研究性学习小组模拟工业法对铝片表面进行氧化处理。他们的实验步骤如下:
a.铝片的预处理,取出一定大小的铝片,依次用苯、酒精擦洗铝片的表面;
b.用水冲洗经有机物擦洗的铝片,浸入60~70 ℃的2 mol·L-1的NaOH溶液中,以除去原有的氧化膜,约1 min后,取出用水冲洗干净,再用钼酸铵溶液处理以抑制电解生成的氧化铝被硫酸溶解;
c.阳极氧化,以铅为阴极,铝片为阳极,以硫酸溶液为电解液,按照如图连接电解装置,电解40 min后取出铝片,用水冲洗,放在水蒸气中封闭处理20~30 min,即可得到更加致密的氧化膜。
试回答下列问题:
(1)用苯和酒精擦拭铝片的目的:_______________________________,
氢氧化钠溶液处理铝片时反应的离子方程式是____________________________________。
(2)阳极的电极反应式为______________________________。
(3)下列有关说法正确的是________(填字母代号)。
A.电解时电子从电源负极→导线→铅极,铝极→导线→电源正极
B.在电解过程中,H+向阳极移动,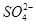 向阴极移动
向阴极移动
C.电解过程中溶液的pH基本不变
D.电解时,铝片为阳极,被氧化
Ⅱ.另一小组针对铝表面保护膜的保护作用展开了研究,他们查阅有关资料得知:尽管铝表面致密的氧化膜能使铝与其周围的介质(空气、水等)隔绝,对铝制品起到保护作用,但铝制容器仍不能长期用来盛放和腌制咸菜。究其原因,该小组设计了一个实验以探究其中的原因。他们的实验过程如下:
|
实验 |
|
|
|
编号 |
实验过程 |
实验现象 |
|
1 |
取一小片铝片于试管中,加入1.0 mol·L-1的盐酸2 mL |
30秒时开始有少量气泡,然后产生气泡的速率加快,最后铝片消失 |
|
2 |
取一小片铝片于试管中,加入0.5 mol·L-1的硫酸2 mL |
55秒时开始有少量气泡,然后产生气泡的速率加快,最后铝片消失 |
|
3 |
取一小片铝片于试管中,加入氯化铜稀溶液 |
3分钟左右表面产生少量气泡,且铝表面析出一些红色固体 |
|
4 |
取一小片铝片于试管中,加入硫酸铜稀溶液 |
一直没有明显的变化 |
你认为实验1、2中盐酸和硫酸的浓度分别为1.0 mol·L-1、0.5 mol·L-1的原因是________________________________________________________________________。
根据该实验现象,你认为铝制容器不能长期盛放和腌制咸菜的原因是________________________________________________________________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com