
题目列表(包括答案和解析)
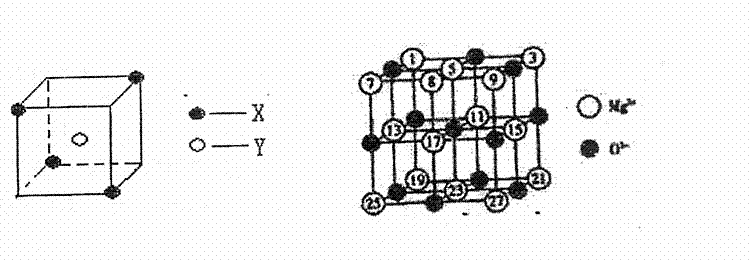
某离子晶体晶胞结构如右图所示,X位于立方体的顶点,Y位于立方体的中心,试回答:
(1)晶体中每个Y同时吸引着 个X,每个X同时吸引着 个Y,该晶体的化学式为 。
(2)晶体中在每个X周围与它最接近且距离相等的X共有 个。
(3)晶体中距离最近的2个X与一个Y形成的夹角(∠XYX)为(填角的度数) 。
(4)设该晶体的摩尔质量为M g?mol-1,晶体密度为ρg?cm-3,阿伏加德罗常数为NA,则晶体中两个距离最近的X中心间的距离为 cm。
(1)某离子晶体晶胞结构单元如图所示,X位于立方体的顶点,Y位于立方体的中心
①晶体中每个Y同时吸引着 个X,每个X同时吸引着 个Y,该晶体的化学式是 。
②晶体中每个X周围与它最接近且距离相等的X共有 个。
③某气态分子也具有上图所示的空间结构,该分子的化学式是 。
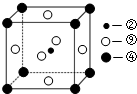
![]() (2)已知MEO的晶体结构属于NaC1型。某同学画出的MgO晶胞结构示意图如右图所示,请改正图中错误: .
(2)已知MEO的晶体结构属于NaC1型。某同学画出的MgO晶胞结构示意图如右图所示,请改正图中错误: .
![]()
![]()
(10分)1915年诺贝尔物理学奖授予Henry Bragg和Lawrence Bragg,以表彰他们用X射线对晶体结构的分析所作的贡献。
(一)科学家通过X射线探明,NaCl、KCl、MgO、CaO晶体结构相似,其中三种晶体的晶格能数据如下表:
|
晶体 |
NaCl |
KCl |
CaO |
|
晶格能/(kJ·mol-1) |
786 |
715 |
3401 |
四种晶体NaCl、KCl、MgO、CaO熔点由高到低的顺序是
(二)科学家通过X射线推测胆矾中微粒间的作用力,胆矾的结构示意图可简单表示如下:

(1)胆矾晶体中含有 (填字母代号)
A.配位键 B.离子键 C.极性共价键
D. 金属键 E.氢 键 F.非极性共价键
(2)Cu2+还能与NH3、Cl-等形成配位数为4的配合物,已知[Cu(NH3)4]2+具有对称的空间构型,[Cu(NH3)4]2+中的两个NH3被两个Cl-取代,能得到两种不同结构的产物,则[Cu(NH3)4]2+的空间构型为 。
(3)金属铜采用下列 (填字母代号)堆积方式。

(4)右图是铜的某种氧化物的晶胞结构示意图,该晶体的密度为a g/cm3,设阿伏伽德罗常数的值为NA,则该晶胞的体积为 cm3

晶体具有规则的几何外形,晶体中最基本的重复单位称为晶胞。
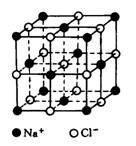 NaCl晶体结构如右图所示。已知FexO晶体晶胞结构为NaCl型,由于晶体缺陷,x值小于1。测知FexO晶体密度为ρg/cm3,晶胞边长为4.28×10-10m。
NaCl晶体结构如右图所示。已知FexO晶体晶胞结构为NaCl型,由于晶体缺陷,x值小于1。测知FexO晶体密度为ρg/cm3,晶胞边长为4.28×10-10m。
⑴FexO中x值(精确至0.01)为___________。
⑵晶体中的Fe分别为Fe2+、Fe3+,在Fe2+和Fe3+的总数中,Fe2+所 占分数(用小数表示,精确至0.001)为___________。
⑶此晶体化学式为____________。
⑷与某个Fe2+(或Fe3+)距离最近且等距离的O2-围成的空间几何构型形状是__________。
⑸在晶体中,铁元素的离子间最短距离为__________m。
| ① | |||||||||||||||||
| ② | ③ | ||||||||||||||||
| ④ | ⑤ | ⑥ | ⑦ | ||||||||||||||
| ⑧ | ⑨ | ⑩ |
| 电离能I(eV) | A | B | C | D | E | F |
| I1 | 11.3 | 14.5 | 13.6 | 5.2 | 7.6 | 6.0 |
| I2 | 24.4 | 29.6 | 35.1 | 49.3 | 15.0 | 18.8 |
| I3 | 47.9 | 47.4 | 54.9 | 71.6 | 80.1 | 28.4 |
| I4 | 64.5 | 77.5 | 77.4 | 98.9 | 109.2 | 112.0 |
| I5 | 392.1 | 97.9 | 113.9 | 138.3 | 141.3 | 153.7 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com