本题分两个题目.
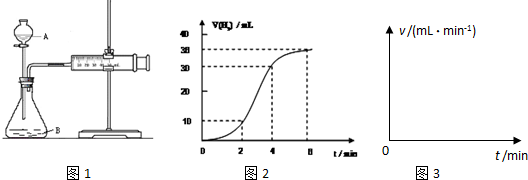
Ⅰ、影响化学反应速率的因素很多,某课外兴趣小组用实验的方法通过图1所示装置研究反应速率的有关问题.
(1)现设计如下实验方案探究温度和c(H
2SO
4)对锌与稀硫酸反应速率的影响.
①请在表格空白处填写适当的反应条件.
| 编号 |
实验目的 |
锌粒 |
温度 |
c(H2SO4) |
需测量的数据 |
| Ⅰ |
为以下实验作参照 |
3粒 |
25℃ |
c1 |
a |
| Ⅱ |
探究温度对反应速率的影响 |
3粒 |
50℃ |
c1 c1 |
b |
| Ⅲ |
探究浓度对反应速率的影响 |
3粒 |
25℃ 25℃ |
c2 |
d |
(注:在实验Ⅰ、Ⅱ、Ⅲ中,锌粒表面积相同)
②“需测量的数据”是
一定时间内收集到的气体体积或收集一定体积的气体所需要的时间
一定时间内收集到的气体体积或收集一定体积的气体所需要的时间
.
(2)对于实验Ⅰ,锌粒与H
2SO
4反应生成H
2的量与反应时间的关系曲线如图2所示.请在图3中画出上述反应的速率(mL/min)与时间(min)的关系曲线图.
Ⅱ、在一定温度下,有a.盐酸 b.硫酸 c.醋酸三种酸.在不同情况下可能有以下关系:
A.b>a>c B.b>a=c C.c>a>b D.c>a=b E.a=b>c
请从上述选项中选择合适的答案.
(3)当三种酸溶液pH相同时,三者物质的量浓度关系顺序是
C
C
.
(4)同体积、同物质的量浓度的三种酸,中和NaOH的能力由大到小的顺序是
B
B
.
(5)当三者c(H
+)相同、体积相同时,同时加入形状、密度、质量完全相同的锌,若产生相同体积的H
2(相同状况),反应所需时间的长短关系是
D
D
(认为H
2SO
4第二步电离完全,并忽略阴离子对反应速率的影响).
(6)将pH相同的三种酸均加水稀释至原来的100倍后,c(H
+)由大到小的顺序是
D
D
.

