
题目列表(包括答案和解析)


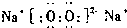
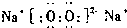
原子序数从小到大排列的四种短周期元素W、X、Y、Z,四种元素的原子最外层电子数之和等于12;W是原子半径最小的元素;由X、Y元素可组成非极性分子A,A在常温下为气体;由Y、Z元素按原子个数比1:1可组成离子化合物B;A与B反应可生成Y2气体.
(1)元素W是:________;
(2)写出金属镁在A中燃烧的化学方程式:________________
该反应属于________(填写序号)
a.置换反应
b.化合反应
c.分解反应
d.复分解反应
e.氧化还原反应
(3)C是由X、Y、Z三种元素组成的盐,C能与盐酸反应生成A,则C的化学式是__________________
(4)D是由W、X、Y三种元素按原子个数比为1∶1∶2组成的一种酸,D在常温下为固体.已知在含1 mol D的水溶液中加入1 mol C恰好反应生成1 mol A.则D的化学式是________;D能使高锰酸钾酸性溶液褪色,说明D具有________性.
三种短周期元素X、Y、Z,它们的原子序数之和为16,X、Y、Z三种元素的常见单质在常温下都是无色气体。已知X原子的最外层电子数是内层电子数的3倍,X和Y的单质直接化合形成气体A,X和Z的单质直接化合形成液态化合物B,Y和Z的单质直接化合形成的化合物C是一种无色有刺激性气味的气体。
请回答下列问题:
(1)Y元素在周期表中的位置是??????? 。
(2)C可在X的单质中燃烧得到Y的单质和化合物B,利用此反应可制成新型的化学电源(KOH溶液做电解质溶液),两个电极均由多孔碳制成,通人的气体由孔隙中逸出,并在电极表面放电,则正极通入的物质是??????? (填物质名称);负极的电极反应式为???????????? ????????? 。
(3)C与X的单质反应生成A的化学方程式为?????????? 。
(4)常温下,C的水溶液的pH=12,则该溶液中由水电离的C(OH-)= ???? 。若向C溶液中加入等体积、等物质的量浓度的盐酸,所得溶液中水的电离程度?????? (填“大于”、“等于”或“小于”)相同条件下C溶液中水的电离程度。
(5)在2L密闭容器中放入1molC气体,在一定温度进行如下反应:
2C(g)  Y2(g)+3Z2(g),反应时间(t)与容器内气体总压强(p)的数据见下表
Y2(g)+3Z2(g),反应时间(t)与容器内气体总压强(p)的数据见下表
时间t/min | 0 | 1 | 2 | 3 | 4 | 5 |
总压强P l00 kPa | 4 | 4.6 | 5.4 | 5.8 | 6 | 6 |
该反应的化学平衡常数表达式是????????????? (用具体物质的化学式表示);平衡时C的转化率为???????????? 。
(6)已知:①Y2(g)+2X2(g)=2YX2(g)?  H=+67.7 kJ·mol-1。
H=+67.7 kJ·mol-1。
②Y2Z4(g)+X2(g)=Y2(g)+2Z2X(g)???  H=-534 kJ·mol-1。
H=-534 kJ·mol-1。
则2Y2Z4(g)+2YX2(g)=3Y2(g)+4Z2X(g)?  H=???? kJ·mol-1
H=???? kJ·mol-1
三种短周期元素X、Y、Z,它们的原子序数之和为16,X、Y、Z三种元素的常见单质在常温下都是无色气体。已知X原子的最外层电子数是内层电子数的3倍,X和Y的单质直接化合形成气体A,X和Z的单质直接化合形成液态化合物B,Y和Z的单质直接化合形成的化合物C是一种无色有刺激性气味的气体。
请回答下列问题:
(1)Y元素在周期表中的位置是 。
(2)C可在X的单质中燃烧得到Y的单质和化合物B,利用此反应可制成新型的化学电源(KOH溶液做电解质溶液),两个电极均由多孔碳制成,通人的气体由孔隙中逸出,并在电极表面放电,则正极通入的物质是 (填物质名称);负极的电极反应式为 。
(3)C与X的单质反应生成A的化学方程式为 。
(4)常温下,C的水溶液的pH=12,则该溶液中由水电离的C(OH-)= 。若向C溶液中加入等体积、等物质的量浓度的盐酸,所得溶液中水的电离程度 (填“大于”、“等于”或“小于”)相同条件下C溶液中水的电离程度。
(5)在2L密闭容器中放入1molC气体,在一定温度进行如下反应:
2C(g) 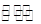 Y2(g)+3Z2(g),反应时间(t)与容器内气体总压强(p)的数据见下表
Y2(g)+3Z2(g),反应时间(t)与容器内气体总压强(p)的数据见下表
| 时间t/min | 0 | 1 | 2 | 3 | 4 | 5 |
| 总压强P l00 kPa | 4 | 4.6 | 5.4 | 5.8 | 6 | 6 |
 H=+67.7 kJ·mol-1。
H=+67.7 kJ·mol-1。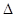 H="-534" kJ·mol-1。
H="-534" kJ·mol-1。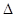 H= kJ·mol-1
H= kJ·mol-1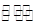 Y2(g)+3Z2(g),反应时间(t)与容器内气体总压强(p)的数据见下表
Y2(g)+3Z2(g),反应时间(t)与容器内气体总压强(p)的数据见下表| 时间t/min | 0 | 1 | 2 | 3 | 4 | 5 |
| 总压强P l00 kPa | 4 | 4.6 | 5.4 | 5.8 | 6 | 6 |
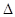 H=+67.7 kJ·mol-1。
H=+67.7 kJ·mol-1。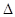 H="-534" kJ·mol-1。
H="-534" kJ·mol-1。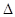 H= kJ·mol-1
H= kJ·mol-1湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com