
题目列表(包括答案和解析)
纳米技术制成的金属燃料、非金属固体燃料、氢气等已应用到社会生活和高科技领域。单位质量的A和B单质燃烧时均放出大量热,可用作燃料。已知A和B为短周期元素,其原子的第一至第四电离能如下表所示:
电离能(kJ/mol) | I1 | I2 | I3 | I4 |
A | 932 | 1821 | 15390 | 21771 |
B | 738 | 1451 | 7733 | 10540 |
(1)某同学根据上述信息,推断B的核外电子排布如图所示,该同学所画的电子排布图违背了????????? 。
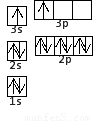
(2)ACl2分子中A的杂化类型为???????? 。
(3)我国部分城市雾霾天占全年一半,引起雾霾的PM2.5微细粒子包含(NH4)2SO4、NH4NO3、有机颗粒物及扬尘等,其中SO42-的空间构型是??????????? (用文字描述),与NO3-互为等电子体的分子是?????????? 。
(4)科学家把C60和钾掺杂在一起制造了一种富勒烯化合物, 其晶胞如图所示,该物质在低温时是一种超导体。写出基态钾原子的价电子排布式????????? ,该物质的K原子和C60分子的个数比为?????????? 。

(5)继C60后,科学家又合成了Si60、N60,C、Si、N原子电负性由大到小的顺序是?????????? 。Si60分子中每个硅原子只跟相邻的3个硅原子形成共价键,且每个硅原子最外层都满足8电子稳定结构,则Si60分子中π键的数目为?????? 。
叠氮化钠(NaN3)是一种无色晶体,常见的两种制备方法为2NaNH2+N2O=NaN3+NaOH+NH3,3NaNH2+NaNO3=NaN3+3NaOH+NH3↑。
回答下列问题:
(1)氮所在的周期中,电负性最大的元素是________,第一电离能最小的元素是_______。
(2)基态氮原子的L层电子排布图为_______________。
(3)与N3-互为等电子体的分子为__________(写出一种)。依据价层电子对互斥理论,NO3-的空间构型为_____________。
(4)氨基化钠(NaNH2)和叠氮化钠(NaN3)的晶体类型为_________________。叠氮化钠的水溶液呈碱性,用离子方程式表示其原因:_____________________________。
 (5)N2O沸点(-88.49℃)比NH3沸点(-33.34℃)低,其主要原因是__________________。
(5)N2O沸点(-88.49℃)比NH3沸点(-33.34℃)低,其主要原因是__________________。
(6)安全气囊的设计原理为6NaN3+Fe2O3?  3Na2O+2Fe+9N2↑。
3Na2O+2Fe+9N2↑。
①氮分子中σ键和π键数目之比为________________________。
②铁晶体中存在的化学键类型为__________________________。
③铁晶体为体心立方堆积,其晶胞如图所示,晶胞边长为a cm,该铁晶体密度为___________(用含a、NA的表达式表示,其中NA为阿伏加德罗常数)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com