
题目列表(包括答案和解析)
向10mL0.1mol·L-1AlCl3溶液中加入40mL0.1 mol·L-1NaAlO2溶液,均匀混合后,铝元素存在的主要形式有 ( )
A.Al(OH)3 B.Al3+和AlO2-
C.Al(OH)3和AlO2- D.Al3+和Al(OH)3
向10ml0.1mol/l的Na[Al(OH)4]溶液中滴加0.1mol/l的HCl溶液,生成沉淀的量与加入的盐酸体积的关系如图
(1)写出OA段的离子方程式
(2)写出AB段的化学方程式
(3)OB段反应共消耗 ml盐酸溶液;
此过程中生成沉淀最多时,沉淀物质的量是 mol,此时消耗的盐酸是 ml
(7分)向10ml0.1mol/l的Na[Al(OH)4]溶液中滴加0.1mol/l的HCl溶液,生成沉淀的量与加入的盐酸体积的关系如图

(1)写出OA段的离子方程式
(2)写出AB段的化学方程式
(3)OB段反应共消耗 ml盐酸溶液;
此过程中生成沉淀最多时,沉淀物质的量是 mol,此时消耗的盐酸是 ml
下列离子方程式不正确的是( )
A.向100mL0.1mol/L 的溴化亚铁溶液中通入0.05mol的氯气时发生反应的离子方程式:2Fe2++4Br-+3Cl2=2 Fe3++2Br2+6Cl-
B.向NH4Al(SO4)2溶液中滴入Ba(OH)2溶液恰好使SO42—完全沉淀:2Ba2++NH4++Al3++2SO42—+4OH-== Al(OH)3↓+NH3·H2O+2BaSO4↓
C.用侯氏制碱法制得NaHCO3 Na++NH3+CO2+H2O=NaHCO3↓+NH4+
D.将Na2O2固体投入H218O中:2H218O+2Na2O2=4OH-+4Na++18O2↑
(7分)向10ml0.1mol/l的Na[Al(OH)4]溶液中滴加0.1mol/l的HCl溶液,生成沉淀的量与加入的盐酸体积的关系如图
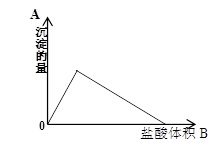
(1)写出OA段的离子方程式
(2)写出AB段的化学方程式
(3)OB段反应共消耗 ml盐酸溶液;
此过程中生成沉淀最多时,沉淀物质的量是 mol,此时消耗的盐酸是 ml
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com