
题目列表(包括答案和解析)
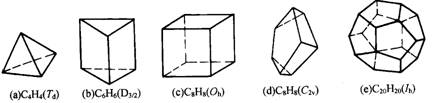
原子簇化学是当前化学中最饶有兴趣而又极其活跃的领域之一。当前比较全面的定义是由徐光宪、江元生等人提出的:凡以3个或3个以上原子直接键合构成的多面体或笼为核心,连接外围原子或基团而形成的结构单元称原子簇.分子式为CnHn的多面体碳烷是典型的主族簇合物,下面是已经报道的碳烷多面体,请归纳总键数为 ;若多面体边数为l,则总键数用n和l表示为多少
 2.端木守拙科研课题是“碱金属卤化物的分子动力学模拟”,研究了体积较大的碱金属卤化物离子簇。从NaCl晶体中可以抽取出不同形状的晶体小碎片,这些晶体小碎片可以称为NaCl离子团簇。离子晶体或离子团簇表面存在悬挂键(即表面的离子有一种没有抓住相邻原子的化学键)。
2.端木守拙科研课题是“碱金属卤化物的分子动力学模拟”,研究了体积较大的碱金属卤化物离子簇。从NaCl晶体中可以抽取出不同形状的晶体小碎片,这些晶体小碎片可以称为NaCl离子团簇。离子晶体或离子团簇表面存在悬挂键(即表面的离子有一种没有抓住相邻原子的化学键)。
右图是立方体形状的NaCl离子团簇,其中大球代表Cl-,小球表代Na+。请回答下列问题:
①与等质量的NaCl离子晶体相比,NaCl离子团簇具有_______(填“较多”或“较少”)的悬挂键;
②NaCl离子团簇的熔点比NaCl大块晶体的熔点要______(填“高”、“低”或“―样”);
③如果团簇中离子对数相同,则团簇的总能量与团簇的外形是否有关 。
④(NaCl)864立方体离子簇的边长相当于 个NaCl单胞的边长。
⑤但是体积小的团簇有特殊性。Na5Cl4+无法形成面心立方结构,它的几种结构中,最稳定的是具有高对称性的平面结构,请画出其结构式
![]() 我国中医药已逐步进入国际市场,但国外在进口中药时对中草药中的重金属元素和有毒元素的含量等各项指标检查是非常严格的。下面是某分析实验室对中草药中可能的残余有毒元素As的检验方法和步骤(As在中草药中主要以As2O3的形式存在):
我国中医药已逐步进入国际市场,但国外在进口中药时对中草药中的重金属元素和有毒元素的含量等各项指标检查是非常严格的。下面是某分析实验室对中草药中可能的残余有毒元素As的检验方法和步骤(As在中草药中主要以As2O3的形式存在):
![]() ①取1.000 kg中草药样品进行灼烧、溶解、过滤等操作制得待测溶液,此时样品中可能含有的As元素将转化为H3AsO3;
①取1.000 kg中草药样品进行灼烧、溶解、过滤等操作制得待测溶液,此时样品中可能含有的As元素将转化为H3AsO3;
![]() ②将待测溶液转移入250 mL锥形瓶中,并加入2~3滴0.2%的淀粉溶液;
②将待测溶液转移入250 mL锥形瓶中,并加入2~3滴0.2%的淀粉溶液;
![]() ③用标准碘溶液滴定待测溶液至终点,消耗20.25 mL标准I2溶液,其间发生反应:
③用标准碘溶液滴定待测溶液至终点,消耗20.25 mL标准I2溶液,其间发生反应:
![]() H3AsO3+I2+H2O―→H3AsO4+I-+H+(未配平)
H3AsO3+I2+H2O―→H3AsO4+I-+H+(未配平)
![]() 试回答下列问题:
试回答下列问题:
![]() (1)过滤时需用的玻璃仪器是: 。
(1)过滤时需用的玻璃仪器是: 。
![]() (2)配平离子反应方程式:[ ]H3AsO3+[ ]I2+[ ]H2O===[ ]H3AsO4+[ ]I-+[ ]H+
(2)配平离子反应方程式:[ ]H3AsO3+[ ]I2+[ ]H2O===[ ]H3AsO4+[ ]I-+[ ]H+
![]() (3)判断滴定到达终点的现象是: 。
(3)判断滴定到达终点的现象是: 。
![]() (4)题中所用标准碘溶液并非将碘单质直接溶解于蒸馏水中制得,而是由0.107 0 g纯KIO3、过量的KI以及酸混合,并将其准确稀释到1 000 mL而制得,请用一个离子反应方程式说明标准碘溶液的形成过程: 。
(4)题中所用标准碘溶液并非将碘单质直接溶解于蒸馏水中制得,而是由0.107 0 g纯KIO3、过量的KI以及酸混合,并将其准确稀释到1 000 mL而制得,请用一个离子反应方程式说明标准碘溶液的形成过程: 。
![]() (5)我国《药用植物及制剂进出口绿色行业标准》中限定:绿色中药的砷含量不超过2.000 mg/kg,计算可知该样品中砷含量约为 mg/kg,故该中草药样品 (填“合格”或“不合格”)。
(5)我国《药用植物及制剂进出口绿色行业标准》中限定:绿色中药的砷含量不超过2.000 mg/kg,计算可知该样品中砷含量约为 mg/kg,故该中草药样品 (填“合格”或“不合格”)。
 我国中医药已逐步进入国际市场,但国外在进口中药时对中草药中的重金属元素和有毒元素的含量等各项指标检查是非常严格的。下面是某分析实验室对中草药中可能的残余有毒元素As的检验方法和步骤(As在中草药中主要以As2O3的形式存在):
我国中医药已逐步进入国际市场,但国外在进口中药时对中草药中的重金属元素和有毒元素的含量等各项指标检查是非常严格的。下面是某分析实验室对中草药中可能的残余有毒元素As的检验方法和步骤(As在中草药中主要以As2O3的形式存在): ①取1.000 kg中草药样品进行灼烧、溶解、过滤等操作制得待测溶液,此时样品中可能含有的As元素将转化为H3AsO3;
①取1.000 kg中草药样品进行灼烧、溶解、过滤等操作制得待测溶液,此时样品中可能含有的As元素将转化为H3AsO3; ②将待测溶液转移入250 mL锥形瓶中,并加入2~3滴0.2%的淀粉溶液;
②将待测溶液转移入250 mL锥形瓶中,并加入2~3滴0.2%的淀粉溶液; ③用标准碘溶液滴定待测溶液至终点,消耗20.25 mL标准I2溶液,其间发生反应:
③用标准碘溶液滴定待测溶液至终点,消耗20.25 mL标准I2溶液,其间发生反应: H3AsO3+I2+H2O―→H3AsO4+I-+H+(未配平)
H3AsO3+I2+H2O―→H3AsO4+I-+H+(未配平) 试回答下列问题:
试回答下列问题: (1)过滤时需用的玻璃仪器是: 。
(1)过滤时需用的玻璃仪器是: 。 (2)配平离子反应方程式:[ ]H3AsO3+[ ]I2+[ ]H2O===[ ]H3AsO4+[ ]I-+[ ]H+
(2)配平离子反应方程式:[ ]H3AsO3+[ ]I2+[ ]H2O===[ ]H3AsO4+[ ]I-+[ ]H+ (3)判断滴定到达终点的现象是: 。
(3)判断滴定到达终点的现象是: 。 (4)题中所用标准碘溶液并非将碘单质直接溶解于蒸馏水中制得,而是由0.107 0 g纯KIO3、过量的KI以及酸混合,并将其准确稀释到1 000 mL而制得,请用一个离子反应方程式说明标准碘溶液的形成过程: 。
(4)题中所用标准碘溶液并非将碘单质直接溶解于蒸馏水中制得,而是由0.107 0 g纯KIO3、过量的KI以及酸混合,并将其准确稀释到1 000 mL而制得,请用一个离子反应方程式说明标准碘溶液的形成过程: 。 (5)我国《药用植物及制剂进出口绿色行业标准》中限定:绿色中药的砷含量不超过2.000 mg/kg,计算可知该样品中砷含量约为 mg/kg,故该中草药样品 (填“合格”或“不合格”)。
(5)我国《药用植物及制剂进出口绿色行业标准》中限定:绿色中药的砷含量不超过2.000 mg/kg,计算可知该样品中砷含量约为 mg/kg,故该中草药样品 (填“合格”或“不合格”)。(A)【物质结构与性质】
下表是元素周期表的一部分。表中所列的字母分别代表某一种化学元素。
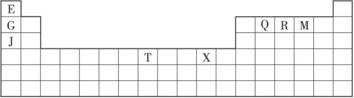
(1)T3+的核外电子排布式是____________。
(2)Q、R、M的第一电离能由大到小的顺序是___________________(用元素符号表示)。
(3)下列有关上述元素的说法中,正确的是______________________(填序号)。
①G单质的熔点高于J单质,是因为G单质的金属键较强
②J比X活泼,所以J可以在溶液中置换出X
③将J
④RE3沸点高于QE4,主要是因为前者相对分子质量较大
⑤一个Q2E4分子中含有五个σ键和一个π键
(4)加拿大天文台在太空发现了EQ9R,已知分子中所有原子均形成8电子或2电子稳定结构,是直线形分子,不存在配位键。写出其结构式:_________________。
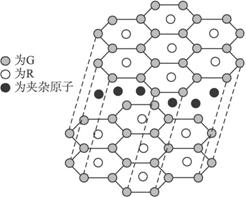
(5)G与R单质直接化合生成一种离子化合物G3R。该晶体具有类似石墨的层状结构。每层中,G原子构成平面六边形,每个六边形的中心有一个R原子。层与层之间还夹杂一定数量的原子。请问这些夹杂的原子应该是____________(填G或R的元素符号)。
(B)【实验化学】
某资料显示,能使双氧水分解的催化剂有很多种,生物催化剂(如猪肝)、离子型催化剂(如FeCl3)和固体催化剂(如MnO2)等都是较好的催化剂。某实验小组通过测定双氧水分解产生的O2的压强,探究分解过氧化氢的最佳催化剂以及探究最佳催化剂合适的催化条件。
(一)探究一:
实验步骤
(1)往锥形瓶中加入50 mL 1.5%的双氧水
(2)分别往锥形瓶中加
(3)采集和记录数据。
(4)整理数据得出下表
不同催化剂“压强对时间斜率”的比较
催化剂 | 猪肝 | 马铃薯 | 氯化铜 | 氯化铁 | 氧化铜 | 二氧化锰 |
压强对时间的斜率 | 0.191 87 | 0.002 42 | 0.007 93 | 0.030 5 | 0.015 47 | 1.833 6 |
①该“探究一”实验的名称是_____________________________________________________。
②该实验所得出的结论是_______________________________________________________。
(二)探究二:二氧化锰催化的最佳催化条件
该实验小组的同学在进行探究二的实验时,得到了一系列的图表和数据。参看下图和表格分别回答相关问题。
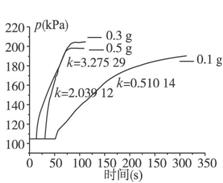
3%的双氧水与不同用量二氧化锰的压力—时间图
表:不同浓度的双氧水在不同用量的二氧化锰作用下收集相同状况下同体积O2所需时间
MnO2 时间 H2O2 | |||
1.5% | 223 s | 67 s | 56 s |
3.0% | 308 s | 109 s | 98 s |
4.5% | 395 s | 149 s | 116 s |
分析图、表中数据我们可以得出:
③同浓度的双氧水的分解速率随着二氧化锰用量的增加而_________________,因而反应时间_______________。
④如果从实验结果和节省药品的角度综合分析,你认为当我们选用3.0%的双氧水,加入___________ g的二氧化锰能使实验效果最佳。你判断的理由是______________________。
⑤该小组的某同学通过分析数据得出了当催化剂用量相同时双氧水的浓度越小反应速率越快的结论,你认为是否正确____________,你的理由是________________________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com