
题目列表(包括答案和解析)
| 滴定次数 | 待测溶液体积/ml | 盐酸标准溶液体积/ml | |
| 滴定前刻度 | 滴定后刻度 | ||
| 第一次 | 10.00 | 0.50 | 20.40 |
| 第二次 | 10.00 | 4.00 | 24.10 |
用0.20mol/L盐酸作标准液,中和滴定法测定某烧碱的纯度。若烧碱中不含有与盐酸反应的杂质,试根据实验回答:
(1)准确称取5.0g烧碱样品,所用主要仪器有托盘天平、砝码、药匙、_____________;
(2)将样品配成250ml待测液,需要的主要仪器有烧杯、玻璃棒、胶头滴管、________;
(3)取10.00ml待测液,需要的仪器有 、锥形瓶;
(4)该实验滴定时 手旋转 式滴定管的玻璃活塞, 手不停地摇动锥形瓶,两眼注视 ,直到滴定终点。
(5)根据下表数据,计算被测烧碱溶液的浓度是____________;
| 滴定次数 | 待测溶液体积/ml | 盐酸标准溶液体积/ml | |
| 滴定前刻度 | 滴定后刻度 | ||
| 第一次 | 10.00 | 0.50 | 20.40 |
| 第二次 | 10.00 | 4.00 | 24.10 |
(6)根据上述各数据,计算烧碱的纯度___________;
(7)用蒸馏水洗涤滴定管后,未经润洗就取标准液来滴定待测液,则导致计算出待测液浓度________;若滴定终点读取数据时俯视,则导致计算出待测液浓度________;(填“偏大”“偏小”“无影响”)。

| 滴定次数 | 待测液体积 | 标准KOH溶液体积/ml | 滴定前读数/ml | 滴定后读数/ml | 第一次 | 20.00 | 0.02 | 25.00 | 第二次 | 20.00 | 0.01 | 25.03 | 第三次 | 20.00 | 0.03 | 26.35 | |
某研究性学习小组用0.20mol·L-1的标准NaOH溶液滴定未知浓度的盐酸,其实验探究操作为如下几步:
① 用蒸馏水洗涤碱式滴定管,并立即注入NaOH溶液至“0”刻度线以上
② 固定好滴定管并使滴定管尖嘴充满液体
③ 调节液面至“0”或“0”刻度线稍下,并记下读数
④ 移取20.00mL待测液注入洁净的锥形瓶中,并加入3滴酚酞溶液
⑤ 用标准液滴定至终点,记下滴定管液面读数。
实验结果和真实浓度差别很大,在指导老师帮助下对重点环节进行了反思、分析,请你也参与评价并请回答:
(1)以上步骤有错误的是(填编号) ,该错误操作会导致测定结果(填“偏大”、“偏小”或“无影响”)__________________
(2)步骤⑤中,在记下滴定管液面读数时,滴定管尖嘴有气泡,将导致测定结果(填“偏大”、“偏小”或“无影响”)___________________
(3)判断滴定终点的现象是:锥形瓶中溶液从 色变为 色,且半分钟不变色。
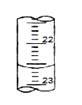
(4)右图是某次滴定时的滴定管中的液面,其读数为 mL
某研究性学习小组用0.20mol·L-1的标准NaOH溶液滴定未知浓度的盐酸,其实验探究操作为如下几步:
① 用蒸馏水洗涤碱式滴定管,并立即注入NaOH溶液至“0”刻度线以上
②固定好滴定管并使滴定管尖嘴充满液体
③ 调节液面至“0”或“0”刻度线稍下,并记下读数
④ 移取20.00mL待测液注入洁净的锥形瓶中,并加入3滴酚酞溶液
⑤ 用标准液滴定至终点,记下滴定管液面读数。
实验结果和真实浓度差别很大,在指导老师帮助下对重点环节进行了反思、分析,请你也参与评价并请回答:
(1)以上步骤有错误的是(填编号) ,该错误操作会导致测定结果(填“偏大”、“偏小”或“无影响”)__________________
(2)步骤⑤中,在记下滴定管液面读数时,滴定管尖嘴有气泡,将导致测定结果(填“偏大”、“偏小”或“无影响”)___________________
(3)判断滴定终点的现象是:锥形瓶中溶液从 色变为 色,且半分钟不变色。
(4)右图是某次滴定时的滴定管中的液面,其读数为 mL
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com