
题目列表(包括答案和解析)
| 名称 | 结构简式 | 常温时的状态 | 熔点/℃ | 沸点/℃ | 相对密度 |
| 甲烷 | CH4 | 气 | -182.5 | -161.5 | |
| 乙烷 | CH3CH3 | 气 | -182.8 | -88.6 | |
| 丙烷 | CH3CH2CH3 | 气 | -188.0 | -42.1 | 0.5005 |
| 戊烷 | CH3(CH2)3CH3 | 液 | -129.7 | 36.0 | 0.5572 |
| 癸烷 | CH3(CH2)8CH3 | 液 | -29.7 | 174.1 | 0.7298 |
| 十七烷 | CH3(CH2)15CH3 | 固 | 22 | 302.2 | 0.7767 |
(08年海南卷)29.(11分)如何防止铁的锈蚀是工业上研究的重点内容。为研究铁锈蚀的影响因素,某同学做了如下探究实验:
序号 | 内容 | 实验现象 |
1 | 常温下将铁丝放在干燥空气中一个月 | 干燥的铁丝表面依然光亮 |
2 | 常温下将铁丝放在潮湿空气中一小时 | 铁丝表面依然光亮 |
3 | 常温下将铁丝放在潮湿的空气中一个月 | 铁丝表面已变得灰暗 |
4 | 将潮湿的铁丝放在常温的氧气流中一小时 | 铁丝表面略显灰暗 |
5 | 将潮湿的铁丝放在高于常温的氧气流中一小时 | 铁丝表面已变得灰暗 |
6 | 将浸过氯化钠溶液的铁丝放在高于常温的氧气流中一小时 | 铁丝表面灰暗程度比实验5严重 |
回答以下问题:
(1)上述实验中发生了电化学腐蚀的是(填实验序号) __________; 在电化学腐 蚀中,负极反应是________________; 正极反应是_______________________;
(2)由该实验可知,可以影响铁锈蚀速率的因素是_________________________;
(3)为防止铁的锈蚀,工业上普遍采用的方法是______________(答两种方法)
(15分)
工业上以磷肥生产形成的副产物石膏(CaSO4·2H2O)与焦炭为原料可生产硫酸,同时可以得到硫酸钾肥料和氯化钙水合物储热材料。以下是有关的工艺流程示意图。
试回答:
(1)写出方程式:反应Ⅰ___________________________________,
(2)写出方程式:反应Ⅱ______________________________________。
(3)请根据下表和化学平衡知识,分析工业上制硫酸中SO2的催化氧化的适宜条件是
____________________________________。
表Ⅰ:
|
转化率/%
温度/℃ | 0.1 | 0.5 | 1 | 10 |
| 400 | 99.2 | 99.6 | 99.7 | 99.9 |
| 500 | 93.5 | 96.9 | 97.8 | 99.3 |
| 600 | 73.7 | 85.8 | 89.5 | 96.4 |
(4)检验滤液H中含有CO的方法是___________________________________。
(5)氯化钙结晶水合物()是目前常用的无机储热材料,选择的依据是___________ (填序号)。
a.熔点较低(29℃熔化) b.能导电 c.易溶于水 d.无毒
(15分)
工业上以磷肥生产形成的副产物石膏(CaSO4·2H2O)与焦炭为原料可生产硫酸,同时可以得到硫酸钾肥料和氯化钙水合物储热材料。以下是有关的工艺流程示意图。
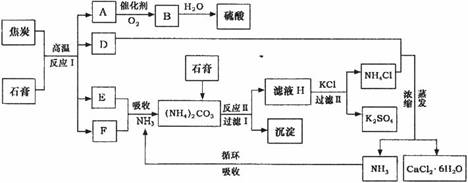
试回答:
(1)写出方程式:反应Ⅰ___________________________________,
(2)写出方程式:反应Ⅱ______________________________________。[来源:ZXXK]
(3)请根据下表和化学平衡知识,分析工业上制硫酸中SO2的催化氧化的适宜条件是
____________________________________。
表Ⅰ:
|
转化率/%
温度/℃ |
0.1 |
0.5 |
1 |
10 |
|
400 |
99.2 |
99.6 |
99.7 |
99.9 |
|
500 |
93.5 |
96.9 |
97.8 |
99.3 |
|
600 |
73.7 |
85.8 |
89.5 |
96.4 |
(4)检验滤液H中含有CO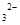 的方法是___________________________________。
的方法是___________________________________。
(5)氯化钙结晶水合物(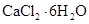 )是目前常用的无机储热材料,选择的依据是___________ (填序号)。
)是目前常用的无机储热材料,选择的依据是___________ (填序号)。
a.熔点较低(29℃熔化) b.能导电 c.易溶于水 d.无毒
(18分)(1)混合动力汽车因具有能量利用率高(95%以上)、节省汽油、发动机噪音低和几乎没有尾气污染等优良性能,受到越来越多的关注,某种混合动力汽车的动力系统由“1.3L汽油机+5速手动变速器+10kw电机+144v镍氢电池”组成。
①汽油机的燃烧之一是乙醇,1克乙醇完全燃烧放出29.7kJ热量,写出乙醇燃烧的热化学方程式 。
②镍氢电池的使用可减少重金属离子污染,其采用储氢金属作为负极,碱液(主要是KOH)作为电解液,镍氢电池充电时发生反应:Ni(OH)2 === NiO(OH)+ H2。其放电时的正极电极反应式为 。
③常温下,浓度同为0.1mol/L的NaHCO3溶液和Na2CO3溶液pH值都大于7,两者中 pH更大,其原因是: 。
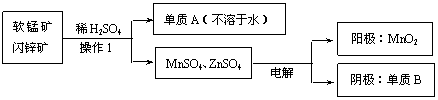
(2)二氧化锰、锌是制造干电池的重要原料,工业上用软锰矿(含MnO2)和闪锌矿(含ZnS)联合生产二氧化锰、锌的工艺如下:
 |
![]()
![]()
![]()
![]()
①操作1的名称为 ,单质A为 ,单质A为 。
![]()
②上述电解过程中,当阴极生成6.5g B时阳极生成的MnO2质量为 。
③利用铝热反应原理,可从软锰矿中提取出单质锰,写出其反应方程式: 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com