
题目列表(包括答案和解析)
①在“烂版液”中逐渐加入6 mol·L-1 NaOH溶液至pH=8为止
②过滤后得到沉淀,用去离子水多次洗涤沉淀
③用 2 mol·L-1的硫酸,保持一定的pH慢慢将沉淀中的Zn(OH)2溶解,加热煮沸,趁热过滤,滤液即为ZnSO4溶液
④溶液中注入2 mol·L-1的硫酸,使其pH保持为2,给溶液……最终制得ZnSO4 ·7H2O
(1)步骤①中测定溶液pH=8的操作是________________。步骤②中如何检验沉淀已经洗涤干净?________________________________________________________________。
(2)步骤③中保持一定pH的目的是____________________________________________。
(3)步骤④还缺少的操作是______________________________________________。
某兴趣小组用废铁泥(主要成分为Fe2O3、FeO和少量Fe)制备磁性Fe3O4纳米材料的流程示意图如下:

|
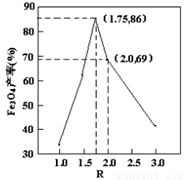
已知:R=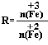 ,步骤⑤中,相同条件下测得Fe3O4的产率与R的关系如图所示。
,步骤⑤中,相同条件下测得Fe3O4的产率与R的关系如图所示。
(1)步骤②中,主要反应的离子方程式是______。
(2)已知:Fe3+在pH=2.8时沉淀完全; Fe2+在pH=6.3时开始沉淀,在pH=8.3时沉淀完全。
步骤③中,用NaOH溶液调pH至9,原因是______。
(3)浊液D中铁元素以FeOOH形式存在。步骤④中,反应的化学方程式是______。
(4)下列说法正确的是______(选填字母)。
a.步骤④中,当反应完成后需再加热一段时间
b.步骤⑤中,反应过程中需要不断补充碱液
c.步骤⑤恰好反应时,n(FeOOH)/n(Fe2+)=2:1
d.当n(浊液D中FeOOH)/n(滤液B中的铁元素)=4/7时,Fe3O4的产率最高
、(12分)钡盐生产中会排出大量的钡泥[主要含有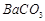 、
、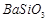 、
、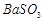 、
、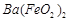 等]。某化工厂主要生产
等]。某化工厂主要生产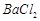 、
、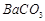 、
、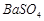 ,现利用钡泥制取
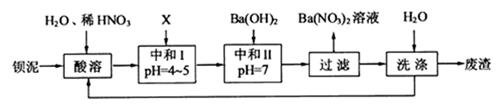
,现利用钡泥制取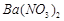 ,其部分工艺流程如下:(已知:(1)FeO2-极易水解而生成Fe(OH)3 (2)Fe3+在pH=3.7时即可水解即沉淀完全)
,其部分工艺流程如下:(已知:(1)FeO2-极易水解而生成Fe(OH)3 (2)Fe3+在pH=3.7时即可水解即沉淀完全)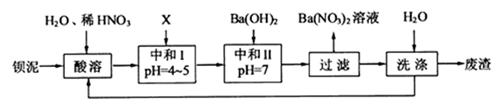
(1)酸溶后溶液中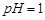 ,
,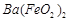 与
与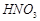 的反应化学方程式为:
的反应化学方程式为:
。
(2)酸溶时通常控制反应温度不超过70℃,且不使用浓硝酸,其原因是防止反应速率过快、浓硝酸挥发且易 。
(3)该厂结合本厂生产实际选用的X为 (填化学式);“中和Ⅰ”会使溶液中(填离子符号) 的浓度减少。
(4)从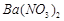 溶液中得到其晶体的分离方法叫 。
溶液中得到其晶体的分离方法叫 。
(5)废渣可直接排放。上述流程中洗涤的目的是 。
用含少量铁的氧化物的氧化铜制取氯化铜晶体(CuCl2 xH2O)。有如下操作:
xH2O)。有如下操作:
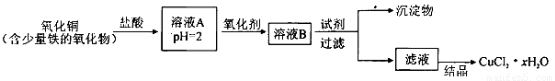
已知:在pH为4~5时,Fe3+几乎完全水解而沉淀,而此时Cu2+却几乎不水解。
(1)溶液A中的金属离子有Fe3+、Fe2+、Cu2+。检验溶液A中Fe2+的最佳试剂为_____(填编号,下同)。
①KMnO4?? ②(NH4)2S??????? ③NaOH???????? ④ KSCN
(2)氧化剂可选用_________。①Cl2? ②KMnO4? ③HNO3? ④H2O2
(3)要得到较纯的产品,试剂可选用_______________。①NaOH ②FeO ③CuO ④Cu2(OH)2CO3
(4)从滤液经过结晶得到氯化铜晶体的方法是_____________(按实验先后顺序选填编号)。
①过滤 ②蒸发浓缩 ③蒸发至干 ④冷却
(5)欲测定溶液A中的Fe2+的浓度,实验前,首先要配制一定物质的量浓度的KMnO4溶液250mL,配制时需要的仪器除天平、玻璃棒、烧杯、药匙、胶头滴管外,还需_________,下列滴定方式中,最合理的是___________(夹持部分略去)(填字母序号)。
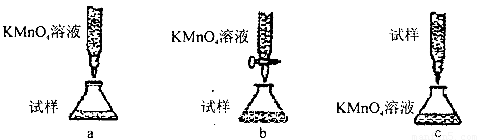
(6)为了测定制得的氯化铜晶体(CuCl2 xH2O)中的x值,某学生设计了两种实验方案:
xH2O)中的x值,某学生设计了两种实验方案:
方案一:称取mg晶体灼烧至质量不再减轻为止,冷却、称量所得无水CuCl2的质量为n1g
方案二:称取mg晶体溶于水,加入足量氢氧化钠溶液、过滤、沉淀洗涤后用小火加热至质量不再减轻为止,冷却,称量所得固体的质量为n2g。
试评价上述两种实验方案:其中正确的方案是________,理由是___________,据此计算得x=_________(用含m、n1或n2的代数式表示)。
、(12分)钡盐生产中会排出大量的钡泥[主要含有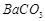 、
、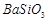 、
、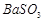 、
、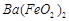 等]。某化工厂主要生产
等]。某化工厂主要生产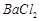 、
、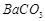 、
、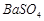 ,现利用钡泥制取
,现利用钡泥制取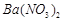 ,其部分工艺流程如下:(已知:(1)FeO2-极易水解而生成Fe(OH)3
(2)Fe3+在pH=3.7时即可水解即沉淀完全)
,其部分工艺流程如下:(已知:(1)FeO2-极易水解而生成Fe(OH)3
(2)Fe3+在pH=3.7时即可水解即沉淀完全)
(1)酸溶后溶液中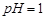 ,
,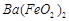 与
与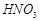 的反应化学方程式为:
的反应化学方程式为:
。
(2)酸溶时通常控制反应温度不超过70℃,且不使用浓硝酸,其原因是防止反应速率过快、浓硝酸挥发且易 。
(3)该厂结合本厂生产实际选用的X为 (填化学式);“中和Ⅰ”会使溶液中(填离子符号) 的浓度减少。
(4)从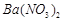 溶液中得到其晶体的分离方法叫
。
溶液中得到其晶体的分离方法叫
。
(5)废渣可直接排放。上述流程中洗涤的目的是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com