
题目列表(包括答案和解析)
编号 | 改变条件 | 合成氨的速率 |
① | 增大N2和H2浓度 |
|
② | 升高温度 |
|
③ | 压缩体积 |
|
④ | 使用铁触媒作催化剂 |
|
⑤ | 容器体积不变,通入氖气 |
|
在固定容积的密闭容器里,进行合成氨的反应:N2(g)+3H2(g)![]() 2NH3(g),当其他条件不变时,只改变一个反应条件,将合成氨的速率的变化填入空格中.
2NH3(g),当其他条件不变时,只改变一个反应条件,将合成氨的速率的变化填入空格中.

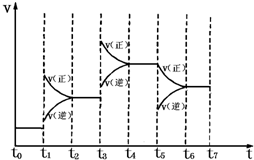 在固定体积的密闭容器中,发生:N2(g)+3H2(g)?2NH3(g)△H=-92.2kJ?mol-1,右图表示在时间t0~t7中反应速率与反应过程的曲线图,则容器内氨的百分含量最高的一段时间是(只改变单一的条件)( )
在固定体积的密闭容器中,发生:N2(g)+3H2(g)?2NH3(g)△H=-92.2kJ?mol-1,右图表示在时间t0~t7中反应速率与反应过程的曲线图,则容器内氨的百分含量最高的一段时间是(只改变单一的条件)( )在固定体积的密闭容器中进行如下反应N2+3H2 ![]() 2NH3 △H<0:,若将平衡体系中各物质的浓度都增大到原来的2倍,则产生的结果是( )
2NH3 △H<0:,若将平衡体系中各物质的浓度都增大到原来的2倍,则产生的结果是( )
①平衡不移动;②平衡右移;③平衡左移;④NH3的百分含量增加;⑤υ(正)、υ(逆)均增大。
A.①⑤ B.①②⑤ C.③⑤ D.②④⑤
在固定体积的密闭容器中,进行如下化学反应:
N2(g)+3H2(g) 2NH3(g)+ Q,其平衡常数K与温度T的关系如下表:
| T/K | 298 | 398 | 498 |
| 平衡常数K | 4.1×106 | K1 | K2 |
①试判断K1 K2(填写“>”“=”或“<”)。
②如果合成氨反应的方程式写为![]() N2(g)+
N2(g)+ ![]() H2(g) NH3(g),其平衡常数为K’,则K’与K的关系为K’ = 。
H2(g) NH3(g),其平衡常数为K’,则K’与K的关系为K’ = 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com