25℃时,几种弱酸溶液的pH如下表所示:
| 弱酸 |
CH3COOH |
H2SO3 |
HCN |
| 物质的量浓度mol/L |
0.01 |
0.01 |
0.01 |
| pH |
3.4 |
2.3 |
5.6 |
(1)25℃时,Na
2SO
3溶液的pH______(填“>”、“<”“或“=”)7,其原因是______(用离子方程式表示).
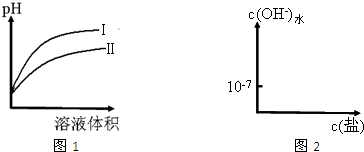
(2)图1是常温下,相同pH的CH
3COOH和HCN溶液分别加水稀释时溶液的pH随溶液体积变化的曲线.
①图1中曲线______(填“Ⅰ”或“Ⅱ”)表示加水稀释HCN溶液时pH的变化.
②下列操作能使CH
3COOH的电离程度与
同时增大的是______.
A.加水稀释溶液 B.升高溶液温度 C.加入少量NaHSO
4固体 D.加入少量CH
3COONa固体
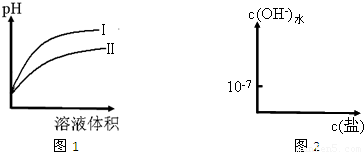
③在图2中分别画出常温下CH
3COONa溶液和NaCN溶液中由水电离出的c(OH
-)与其盐浓度的变化曲线.
(3)常温下,物质的量浓度相同的CH
3COONa溶液和NaCN溶液中,CH
3COONa溶液中各离子浓度之和______(填“>”、“<”或“=”)NaCN溶液中各离子浓度之和.
(4)已知:HCN(aq)
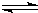
H
+(aq)+CN
-(aq)△H=+43.5kJ?mol
-1H
+(aq)+OH
-(aq)=H
2O(1)△H=-57.3kJ?mol
-1则NaCN在溶液中发生水解的热化学方程式:
CN
-(aq)+H
2O(1)
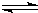
HCN(aq)+OH
-(aq)的△H=______.该反应25℃时的平衡常数K=______.
(需填具体数值,已知10
-5.6=2.5×10
-6)


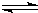
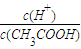 同时增大的是______.
同时增大的是______.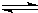 H+(aq)+CN-(aq)△H=+43.5kJ?mol-1
H+(aq)+CN-(aq)△H=+43.5kJ?mol-1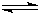 HCN(aq)+OH-(aq)的△H=______.该反应25℃时的平衡常数K=______.
HCN(aq)+OH-(aq)的△H=______.该反应25℃时的平衡常数K=______.![]() H++Ae-)时的pH约为3,如果在此溶液中加入等体积的pH为5的盐酸,则电离平衡__________(填“向左”“向右”“不移动”)。若向原醋酸溶液加入少量醋酸钠晶体,待晶体溶解后溶液的pH值_________(填“增大”“减小”“不变”)。
H++Ae-)时的pH约为3,如果在此溶液中加入等体积的pH为5的盐酸,则电离平衡__________(填“向左”“向右”“不移动”)。若向原醋酸溶液加入少量醋酸钠晶体,待晶体溶解后溶液的pH值_________(填“增大”“减小”“不变”)。