
题目列表(包括答案和解析)

A.(1)在上面元素周期表中画出金属元素与非金属元素的分界线。?
(2)根据NaH的存在,有人提议可将氢元素放在ⅦA族,那么根据其最高正价与最低负价的绝对值相等,又可将氢元素放在周期表中的__________族。?
(3)现有甲、乙两种元素,甲元素原子核外3p亚层上有5个电子,乙元素的焰色反应显黄色。
① 用元素符号将甲、乙两元素填写在上面元素周期表中对应位置。?
②甲元素与硫元素相比较,非金属性较强的是__________(填名称),写出可以验证该结论的一个化学反应方程式__________。
B.
(1)在上面元素周期表中全部是金属元素的区域为__________。?
(a)A (b)B (c)C (d)D
(2)有人认为形成化合物最多的元素不是ⅣA族的碳元素,而是另一种短周期元素,请你根据学过的化学知识判断这一元素是__________。?
(3)现有甲、乙两种短周期元素,室温下,甲元素单质在冷的浓硫酸或空气中,表面都生成致密的氧化膜,乙元素原子核外M电子层与K电子层上的电子数相等。
①用元素符号将甲、乙两元素填写在上面元素周期表中对应的位置。?
②甲、乙两元素相比较,金属性较强的是__________(填名称),可以验证该结论的实验是__________。
(a)将在空气中放置已久的这两种元素的块状单质分别放入热水中?
(b)将这两种元素的单质粉末分别和同浓度的盐酸反应?
(c)将这两种元素的单质粉末分别和热水作用,并滴入酚酞溶液?
(d)比较这两种元素的气态氢化物的稳定性?
(A)

(1)在上面元素周期表中画出金属元素与非金属元素的分界线。
(2)根据NaH的存在,有人提议可把氢元素放在ⅦA族,那么根据其最高正价与最低负价的绝对值相等,又可把氢元素放在周期表中_______族。
(3)现有甲、乙两种元素,甲元素原子核外3p亚层上有5个电子(即M层上有7个电子),乙元素的焰色反应呈黄色。
①用元素符号将甲、乙两元素填写在上面元素周期表中对应的位置。
②甲元素与硫元素相比较,非金属性较强的是______(填名称),写出可以验证该结论的一个化学反应方程式__________。
(B)

(1)在上面元素周期表中全部是金属元素的区域为______。
A.A B.B C.C D.D
(2)有人认为形成化合物最多的元素不是ⅣA族的碳元素,而是另一种短周期元素,请你根据学过的化学知识判断这一元素是______。
(3)现有甲、乙两种短周期元素,室温下,甲元素单质在冷的浓硫酸或空气中,表面都生成致密的氧化膜,乙元素原子核外M电子层与K电子层上的电子数相等。
①用元素符号将甲、乙两元素填写在上面元素周期表中对应的位置。
②甲、乙两元素相比较,金属性较强的是_____(填名称),可以验证该结论的实验是_____。
A.将在空气中放置已久的这两种元素的块状单质分别放入热水中
B.将这两种元素的单质粉末分别和同浓度的盐酸反应
C.将这两种元素的单质粉末分别和热水作用,并滴入酚酞溶液
D.比较这两种元素的气态氢化物的稳定性
(1)(4分)分析下列反应中水的作用。
A.2H2O ![]() 2H2↑+ O2↑ B.2F2 + 2H2O = 4HF + O2
2H2↑+ O2↑ B.2F2 + 2H2O = 4HF + O2
C.Cl2 + H2O ⇌ HCl + HClO D.3 Fe + 4 H2O ![]() Fe3O4+4H2
Fe3O4+4H2
试用相应的反应代号(A.B.C.D.)回答下列问题:H2O只作氧化剂的是________;只作还原剂的是_________;既作氧化剂又作还原剂的是________;既不作氧化剂又不作还原剂的是________。
(2)(2分)写出H2SO4的电离方程式
—1分别中和等量的氢氧化钠溶液,需要a mol/L的盐酸、b mol/L的硝酸、c mol/L的硫酸溶液的体积相等,则a、b、c的关系式正确的是 ( )
A.a = b= c B.2a = 2b = c C.a = b = 2c D.都不正确
(1)分别向盛有等量铜片的四支试管中加入等体积的①浓硫酸②稀硫酸③浓硝酸④稀硝酸,能随即发生剧烈反应的是(填序号,下同)________,常温下缓慢反应(或微热后能发生剧烈反应)的是________,常温下不反应,但加热后发生剧烈反应的是________,加热也不发生反应的是________.由此可以得到上述四种酸氧化性由强到弱的顺序是:________.
(2)工业上用洗净的废铜屑作原料来制备硝酸铜.为了节约原料和防止污染环境,宜采取的方法是________(填序号)
A.Cu+HNO3(浓)![]() Cu(NO3)2
Cu(NO3)2
B.Cu+HNO3(稀)![]() Cu(NO3)2
Cu(NO3)2
C.Cu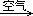 CuO
CuO Cu(NO3)2
Cu(NO3)2
D.Cu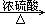 CuSO4
CuSO4 Cu(NO3)2
Cu(NO3)2
(3)先将铜与浓硫酸反应产生的气体X持续通入下图装置中,一段时间后再将铜与浓硝酸反应产生的大量气体Y也持续通入该装置中,可观察到的现象包括________
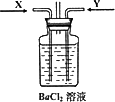
A.通入X气体后产生白色沉淀
B.通入X气体后溶液中无明显现象
C.通入Y气体后开始沉淀
D.通入Y气体后沉淀溶解
E.通入Y气体后溶液中无明显现象
由此可得到的结论是:________
A.HNO3的酸性比H2SO4强
B.盐酸的酸性比H2SO3强
C.BaSO3能溶于盐酸
D.HNO3能氧化H2SO3(或SO2)
E.BaSO4不溶于水也不溶于HNO3溶液
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com