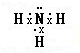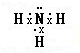(2013?房山区一模)短周期元素A、B、C、D在周期表中的位置如图所示,B、D最外层电子数之和为12,二者可形成DB
2、DB
3两种分子,DB
2具有漂白性.
回答下列问题:
(1)A的氢化物的电子式是
(2)下列叙述中,正确的是
a
a
(填字母)
a.稳定性:A的氢化物>C的氢化物
b.还原性:B
2->D
2-C.酸性:H
4CO
4>H
2DO
4d.最高化合价值:D=B>A>C
(3)DB
2通过下列工艺流程可制化工业原料H
2DB
4和清洁能源H
2.
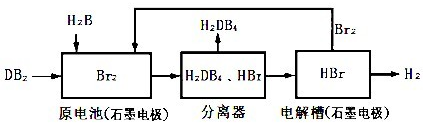
①为摸清电解情况查得:
| 化学键 |
H-H |
Br-Br |
H-Br |
| 能量(kJ/mol) |
436 |
194 |
362 |
试写出通常条件下电解槽中发生总反应的热化学方程式:
2HBr(aq)=H2(g)+Br2(g)△H=+94kJ/mol
2HBr(aq)=H2(g)+Br2(g)△H=+94kJ/mol
②根据资料:
| 化学式 |
Ag2SO4 |
AgBr |
| 溶解度(g) |
0.796 |
8.4×10-6 |
为检验分离器的分离效果,取分离后的H
2DB
4溶液于试管,向其中逐滴加入AgNO
3溶液至充分反应,若观察到
无淡黄色沉淀产生,最终生成白色沉淀
无淡黄色沉淀产生,最终生成白色沉淀
,证明分离效果较好.
③在原电池中,负极发生的反应式为
SO2+2H2O-2e-=4H++SO42-
SO2+2H2O-2e-=4H++SO42-
.
④在电解过程中,电解槽阴极附近溶液pH
变大
变大
(填“变大”、“变小”或“不变”).
⑤将该工艺流程用总反应的化学方程式表示为:
SO2+2H2O=H2SO4+H2
SO2+2H2O=H2SO4+H2
.该生产工艺的优点有
溴可以循环利用,获得清洁能源氢气
溴可以循环利用,获得清洁能源氢气
(答一点即可);缺点有
生成过程有有毒物质,电解循环能源大
生成过程有有毒物质,电解循环能源大
(答一点即可).