
题目列表(包括答案和解析)
铁铜单质及其化合物的应用范围很广。现有含氯化亚铁杂质的氯化铜晶体(CuCl2·2H2O),为制取纯净的CuCl2·2H2O,首先将其制成水溶液,然后按照如图步骤进行提纯:
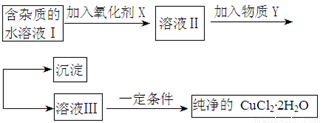
已知Cu2+、Fe3+和Fe2+的氢氧化物开始沉淀和沉淀完全时的pH见下表:
|
|
Fe3+ |
Fe2+ |
Cu2+ |
|
氢氧化物开始沉淀时的pH |
1.9 |
7.0 |
4.7 |
|
氢氧化物沉淀完全时的pH |
3.2 |
9.0 |
6.7 |
请回答下列问题:
(1)加入氧化剂的目的是
(2)下列最适合作氧化剂X的是
A.K2Cr2O7 B.NaClO C.H2O2 D.KMnO4
(3)加入的物质Y是
(4)如果不用物质Y而直接用可溶性碱溶液能不能达到目的? (填“能”或者“不能”)。若不能,试解释原因 (若填“能”,此空不用回答)
(5)最后能不能直接蒸发得到CuCl2·2H2O? (填“能”或者“不能”)。若不能,应该如何操作才能得到CuCl2·2H2O (若填“能”,此空不用回答)
(6)若向溶液Ⅱ中加入碳酸钙,产生的现象是
(7)若向溶液Ⅱ中加入镁粉,产生的气体是 ,试解释原因
(8)FeCl3溶液具有净水作用的原因是
铁铜单质及其化合物的应用范围很广。现有含氯化亚铁杂质的氯化铜晶体(CuCl2·2H2O),为制取纯净的CuCl2·2H2O,首先将其制成水溶液,然后按照如图步骤进行提纯: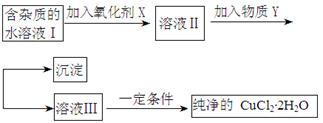
已知Cu2+、Fe3+和Fe2+的氢氧化物开始沉淀和沉淀完全时的pH见下表:
| | Fe3+ | Fe2+ | Cu2+ |
| 氢氧化物开始沉淀时的pH | 1.9 | 7.0 | 4.7 |
| 氢氧化物沉淀完全时的pH | 3.2 | 9.0 | 6.7 |
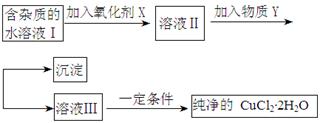
| | Fe3+ | Fe2+ | Cu2+ |
| 氢氧化物开始沉淀时的pH | 1.9 | 7.0 | 4.7 |
| 氢氧化物沉淀完全时的pH | 3.2 | 9.0 | 6.7 |
(分)加碘盐可防止碘缺乏病,目前加碘盐中加入的是碘酸钾。碘酸钾晶体通常情况下有较高的稳定性,但在酸性溶液中,碘酸钾是一种较强的氧化剂,能跟某些还原剂作用生成碘;在碱性溶液中,碘酸钾能被氯气、次氯酸等强氧化剂氧化为更高价的碘的含氧酸盐。工业上制碘酸钾的方法是:将碘单质与氯酸钾混合后加入稀酸酸化加热可反应生成碘酸氢钾及氯化钾、氯气。加热使所有的氯气都逸出。冷却结晶后可得到碘酸氢钾晶体,再溶解于水得到碘酸氢钾溶液。用KOH溶液调节pH值,再蒸发结晶即可得到碘酸钾。
(1)已知下列反应中,两种还原产物所得电子数目相同,请配平该反应的化学方程式:
□I2+□KClO3+□H2O→□KH(IO3)2+□KCl+□Cl2↑。
(2)在生成碘酸氢钾时用稀酸酸化时不能用盐酸,因为盐酸会与碘酸氢钾反应而生成氯气、碘单质及氯化钾,请写出反应的化学方程式 。
(3)如果在得到碘酸氢钾后省略了“加热使所有的氯气都逸出。冷却结晶后可得到碘酸氢钾晶体,再溶解于水得到碘酸氢钾溶液。”直接用KOH溶液调节pH,则可能会导致碘酸钾的产率 ;原因是 。
(4)用题给的方法生产碘酸钾时,得到的碘酸钾23.54g与KClO溶液混合反应后得到的高碘酸钾为23g,试写出反应的离子方程式 ,则该碘酸钾的纯度为
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com