
题目列表(包括答案和解析)
 2NH3(g),若在恒温、恒压条件下向平衡体系中通入氩气,则平衡 移动(填“向左”“向右”或“不”);使用催化剂,上述反应的△H________(填“增大” “减小” 或“不改变”)。
2NH3(g),若在恒温、恒压条件下向平衡体系中通入氩气,则平衡 移动(填“向左”“向右”或“不”);使用催化剂,上述反应的△H________(填“增大” “减小” 或“不改变”)。 式),生成该沉淀的离子方程式为____________。已知25℃时Ksp[Mg(OH)2]=1.8×10-11,Ksp[Cu(OH)2]=2.2×10-20。
式),生成该沉淀的离子方程式为____________。已知25℃时Ksp[Mg(OH)2]=1.8×10-11,Ksp[Cu(OH)2]=2.2×10-20。 中性,则Va︰Vb= 。
中性,则Va︰Vb= 。

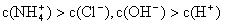

 NH3·H2O + H+,则该反应常温下的平衡常数K= (已知:常温下,NH3·H2O的电离平衡常数Kb=1.7×10—5 mol·L—1)
NH3·H2O + H+,则该反应常温下的平衡常数K= (已知:常温下,NH3·H2O的电离平衡常数Kb=1.7×10—5 mol·L—1)运用化学反应原理研究氮、氧等单质及其化合物的反应有重要意义.
(1)合成氨反应N2(g)+3H2(g)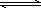 2NH3(g),若在恒温、恒压条件下向平衡体系中通入氩气,则平衡________移动(填“向左”“向右”或“不”);使用催化剂,上述反应的ΔH________(填“增大”“减小”或“不改变”).
2NH3(g),若在恒温、恒压条件下向平衡体系中通入氩气,则平衡________移动(填“向左”“向右”或“不”);使用催化剂,上述反应的ΔH________(填“增大”“减小”或“不改变”).
(2)一氧化碳在高温下与水蒸气反应的方程式为:CO+H2O=CO2+H2.已知部分物质燃烧的热化学方程式如下:
2H2(g)+O2(g)=2H2O(l);ΔH=-571.6 kJ·mol-
2CO(g)+O2(g)=2CO2(g);ΔH=-566 kJ·mol-1
又知1 mol H2O(g)转变为1 mol H2O(l)时放出44.0 kJ热量.写出CO和水蒸气在高温催化剂下反应的热化学方程式________.
(3)在25℃下,向浓度均为0.1 mol?L-1的MgCl2和CuCl2混合溶液中逐滴加入氨水,先生成________沉淀(填化学式),生成该沉淀的离子方程式为________.已知25℃时Ksp[Mg(OH)2]=1.8×10-11,Ksp[Cu(OH)2]=2.2×10-20.
(4)有人设想寻求合适的催化剂和电极材料,以N2、H2为电极反应物,以HCl-NH4Cl为电解质溶液制造新型燃烧电池,放电过程中,溶液中铵根离子浓度逐渐增大.请写出该电池的正极反应式________.
(5)某温度(t℃)时,测得0.01 mol·L-1的NaOH溶液的pH=11.在此温度下,将pH=1的H2SO4溶液VaL与pH=11的NaOH溶液VbL混合,若所得混合液为中性,则Va∶Vb=________.
(6)在25℃下,将a mol·L-1的氨水与0.01 mol·L-1的盐酸等体积混合,反应平衡时溶液中c(NH4+)=c(Cl-).则溶液显________性(填“酸”“碱”或“中”);
(7)NH4Cl是一种重要的化肥.
①用0.1 mol·L-1的盐酸滴定0.1 mol·L-1的氨水,滴定过程中不可能出现的结果是:
a.c(NH![]() )=c(Cl-),c(OH-)=c(H+)
)=c(Cl-),c(OH-)=c(H+)
b.c(NH![]() )>c(Cl-),c(OH-)<c(H+)
)>c(Cl-),c(OH-)<c(H+)
c.c(NH![]() )>c(Cl-),c(OH-)>c(H+)
)>c(Cl-),c(OH-)>c(H+)
d.c(NH![]() )<c(Cl-),c(OH-)>c(H+)
)<c(Cl-),c(OH-)>c(H+)
②NH4Cl溶液中存在:NH4++H2O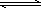 NH3·H2O+H+,则该反应常温下的平衡常数K=________(已知:常温下,NH3·H2O的电离平衡常数Kb=1.7×10-5 mol·L-1)
NH3·H2O+H+,则该反应常温下的平衡常数K=________(已知:常温下,NH3·H2O的电离平衡常数Kb=1.7×10-5 mol·L-1)



湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com