
题目列表(包括答案和解析)
(共10分)
市售乙醛通常为40%左右的乙醛溶液。久置的乙醛溶液会产生分层现象,上层为无色油状液体,下层为水溶液。据测定,上层物质为乙醛的加合物作(C2H4O)n,它的沸点比水的沸点高,分子中无醛基。乙醛在溶液中易被氧化。为从变质的乙醛溶液中提取乙醛(仍得到溶液),可利用如下反应原理:
(1)(1.5分)先把混合物分离得到(C2H4O)n;将混合物放入分液漏斗,分层清晰后,分离操作是_____________。
(2) (1.5分)证明是否已有部分乙醛被氧化的实验操作和现象是_______。
(3) (2分)若将少量乙醛溶液滴入浓硫酸中,生成黑色物质。请用化学方程式表示这一过程: . 。
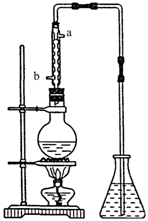 (4) (4分)提取乙醛的装置如下图;烧瓶中放的是(C2H4O)n和6mol/L H2SO4的混合液,锥形瓶中放蒸馏水。加热至混合液沸腾,(C2H4O)n缓慢分解,生成的气体导入锥形瓶的水中。
(4) (4分)提取乙醛的装置如下图;烧瓶中放的是(C2H4O)n和6mol/L H2SO4的混合液,锥形瓶中放蒸馏水。加热至混合液沸腾,(C2H4O)n缓慢分解,生成的气体导入锥形瓶的水中。
① 用冷凝管的目的是 ,冷凝水的进口是 。(填“a”或“b”)。
② 锥形瓶内导管口出现的气泡从下上升到液面的过程中,体积越来越小,直至完全消失,这现象说明乙醇的何种物理性质?
当观察到导管中的气流几小时。必要的操作是:
③ 若n=3,则(C2H4O)n的结构简式是 :
实验室要配制100mL、10mol·L-1的NaCl溶液,试回答下列各题:
(1)(2分)经计算,应该用托盘天平称取NaCl固体 g。
(2)(2分)配制溶液时一般可分为以下几个步骤: ①称量 ②计算 ③定容
④移液 ⑤洗涤 ⑥溶解 其正确的操作顺序为 。
(3)(2分,每空1分)该实验两次用到玻璃棒,其作用分别是:
① 溶解时玻璃棒的作用 ② 移液时玻璃棒的作用
(4)(2分)容量瓶上需标有以下5项中的 ①温度 ②浓度 ③容量 ④压强 ⑤刻度线( )
A.①③⑤ B.③⑤⑥ C.①②④ D.②④⑥
(5)(2分)若用NaCl固体配制溶液,下列仪器中,不需要用到的是_____ 。(填序号)
A.蒸发皿 B.100mL容量瓶 C.烧杯 D.胶头滴管 E.药匙 F.托盘天平 G.玻璃棒
(6)(2分)下列错误操作会导致所得溶液浓度偏低的是 (多项,填序号)。
A. 定容时仰视容量瓶刻度线
B. 容量瓶中原有少量蒸馏水
C. 定容后,把容量瓶倒置摇匀后发现液面低于刻度线,便补充几滴水至刻度处
D. 配制好溶液后,容量瓶未塞好,洒出一些溶液
(12分)有机物A有下列转化关系,已知等物质的量的B和C完全燃烧后产生的CO2的量相等。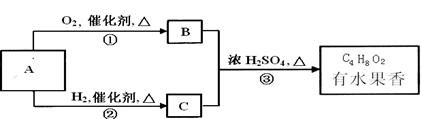
|


|
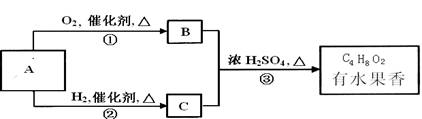
(12分)有机物A有下列转化关系,已知等物质的量的B和C完全燃烧后产生的CO2的量相等。
|

|
(1)物质A和B的结构简式分别是__ __。(每个1分,共2分)
(2)反应①、②、③中,属于取代反应的是___ _(填序号)。(1分)
(3)写出反应②的化学方程式:__ __。(2分)
(4)C4H8O2有多种同分异构体,写出满足下列条件的同分异构体的结构简式:
① 既能发生银镜反应,又能发生酯化反应(5分)
② 既能发生银镜反应,又能发生水解反应(2分)
实验室要配制100mL、10mol·L-1的NaCl溶液,试回答下列各题:
(1)(2分)经计算,应该用托盘天平称取NaCl固体 g。
(2)(2分)配制溶液时一般可分为以下几个步骤: ①称量 ②计算 ③定容
④移液 ⑤洗涤 ⑥溶解 其正确的操作顺序为 。
(3)(2分,每空1分)该实验两次用到玻璃棒,其作用分别是:
① 溶解时玻璃棒的作用 ② 移液时玻璃棒的作用
(4)(2分)容量瓶上需标有以下5项中的 ①温度 ②浓度 ③容量 ④压强 ⑤刻度线( )
A.①③⑤ B.③⑤⑥ C.①②④ D.②④⑥
(5)(2分)若用NaCl固体配制溶液,下列仪器中,不需要用到的是_____。(填序号)
A.蒸发皿 B.100mL容量瓶 C.烧杯 D.胶头滴管 E.药匙 F.托盘天平 G.玻璃棒
(6)(2分)下列错误操作会导致所得溶液浓度偏低的是 (多项,填序号)。
A. 定容时仰视容量瓶刻度线
B.容量瓶中原有少量蒸馏水
C. 定容后,把容量瓶倒置摇匀后发现液面低于刻度线,便补充几滴水至刻度处
D. 配制好溶液后,容量瓶未塞好,洒出一些溶液
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com