
题目列表(包括答案和解析)
已知下列数据:
|
物质 |
熔点(℃) |
沸点(℃) |
密度(g/cm3) |
|
乙醇 |
-117.3 |
78.5 |
0.789 |
|
乙酸 |
16.6 |
117.9 |
1.05 |
|
乙酸乙酯 |
-83.6 |
77.5 |
0.90 |
|
浓硫酸(98%) |
- |
338.0 |
1.84 |
学生在实验室制取乙酸乙酯的主要步骤如下:
①在30 mL的大试管A中按体积比1∶4∶4的比例配制浓硫酸、乙醇和乙酸的混合溶液;
②按下图连接好装置(装置气密性良好),用小火均匀地加热装有混合溶液的大试管5~10 min;
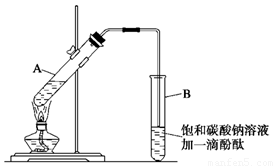
③待试管B收集到一定量的产物后停止加热,撤去试管B并用力振荡,然后静置待分层;
④分离出乙酸乙酯层,洗涤、干燥。
请根据题目要求回答下列问题:
(1)配制该混合溶液的主要操作步骤为____________________________________
写出制取乙酸乙酯的化学方程式: _____________________________________
(2)上述实验中饱和碳酸钠溶液的作用是(填字母)_______________________________。
A.中和乙酸和乙醇
B.中和乙酸并吸收部分乙醇
C.乙酸乙酯在饱和碳酸钠溶液中的溶解度比在水中更小,有利于分层析出
D.加速酯的生成,提高其产率
(3)步骤②中需要小火均匀加热操作,其主要理由是____________________________________
(4)指出步骤③所观察到的现象: _______________________________________________
分离出乙酸乙酯后,为了干燥乙酸乙酯可选用的干燥剂为(填字母)__________。
A.P2O5 B.无水Na2SO4 C.碱石灰 D.NaOH固体
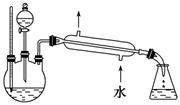
(5)某化学课外小组设计了如下图所示的制取乙酸乙酯的装置(图中的铁架台、铁夹、加热装置已略去),与上图装置相比,此装置的主要优点有: __________________________________
| 物质 | 熔点(℃) | 沸点(℃) | 密度(g/cm3) |
| 乙醇 | -117.0 | 78.0 | 0.79 |
| 乙酸 | 16.6 | 117.9 | 1.05 |
| 乙酸乙酯 | -83.6 | 77.5 | 0.90 |
| 浓硫酸(98%) | - | 338.0 | 1.84 |
| 浓硫酸 |
| 加热 |
| 浓硫酸 |
| 加热 |
已知下列数据:
|
物质 |
熔点/℃ |
沸点/℃ |
密度/g·cm-3 |
|
乙醇 |
-144 |
78 |
0.789 |
|
乙酸 |
16.6 |
117.9 |
1.05 |
|
乙酸乙酯 |
-83.6 |
77.5 |
0.900 |
|
浓H2SO4 |
|
338 |
1.84 |
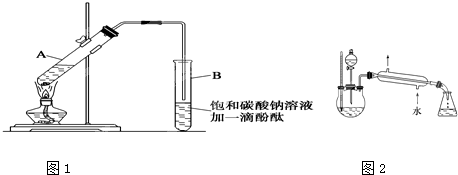
实验室制乙酸乙酯的主要装置如下图(a)所示,主要步骤为:
①在30mL的大试管中按体积比1:4:4的比例配制浓硫酸、乙醇和乙酸的混合液;
②按(a)图连接装置,使产生的蒸气经导管通到15ml试管所盛饱和Na2CO3溶液(加入1滴酚酞试液)上方2mm~3mm处;
③小火加热试管中的混合液;
④待小试管中收集到约4mL产物时停止加热,撤出小试管并用力振荡,然后静置待其分层;
⑤分离出纯净的乙酸乙酯。
请回答下列问题:
(1)步骤①中,配制这一比例的混合液的操作是
(2)写出该反应的化学方程式________,浓H2SO4的作用是________。
(3)步骤③中,用小火加热试管中的混合液,其原因是________。
(4)步骤④所观察到的现象是________,写出原因与结论:________。
(5)步骤⑤中,分离出乙酸乙酯选用的仪器是________,产物应从________口倒出,因为________。
(6)为提高乙酸乙酯的产率,甲、乙两位同学分别设计了如上图甲、乙的装置(乙同学待反应完毕冷却后再用饱和Na2CO3溶液提取烧瓶中产物)。你认为哪种装置合理,为什么?答________。
|
物质 |
熔点/℃ |
沸点/℃ |
密度/g·cm-3 |
|
乙醇 |
-144 |
78 |
0.789 |
|
乙酸 |
16.6 |
117.9 |
1.05 |
|
乙酸乙酯 |
-83.6 |
77.5 |
0.900 |
|
浓H2SO4 |
|
338 |
1.84 |
实验室制乙酸乙酯的主要装置如下图(a)所示,主要步骤为:
①在30mL的大试管中按体积比1:4:4的比例配制浓硫酸、乙醇和乙酸的混合液;
②按(a)图连接装置,使产生的蒸气经导管通到15ml试管所盛饱和Na2CO3溶液(加入1滴酚酞试液)上方2mm~3mm处;
③小火加热试管中的混合液;
④待小试管中收集到约4mL产物时停止加热,撤出小试管并用力振荡,然后静置待其分层;
⑤分离出纯净的乙酸乙酯。
请回答下列问题: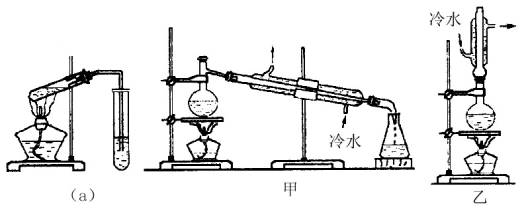
(1)步骤①中,配制这一比例的混合液的操作是
(2)写出该反应的化学方程式________,浓H2SO4的作用是________。
(3)步骤③中,用小火加热试管中的混合液,其原因是________。
(4)步骤④所观察到的现象是________,写出原因与结论:________。
(5)步骤⑤中,分离出乙酸乙酯选用的仪器是________,产物应从________口倒出,因为________。
(6)为提高乙酸乙酯的产率,甲、乙两位同学分别设计了如上图甲、乙的装置(乙同学待反应完毕冷却后再用饱和Na2CO3溶液提取烧瓶中产物)。你认为哪种装置合理,为什么?答________。
已知下列数据:
|
物质 |
熔点代 |
沸点/℃ |
密度/·cm-3 |
|
乙醇 |
-144 |
78 |
0.789 |
|
乙酸 |
16.6 |
117.9 |
1.05 |
|
乙酸乙酯 |
-83.6 |
77.5 |
0.900 |
|
浓H2SO4 |
|
338 |
1.84 |
实验室制乙酸乙酯的主要装置如下图(a)所示,主要步骤为:①在30mL的大试管中按体积比1:4:4的比例配制浓硫酸、乙醇和乙酸的混合液;②按(a)图连接装置,使产生的蒸气经导管通到15ml试管所盛饱和Na2CO3溶液(加入1滴酚酞试液)上方2mm~3mm处;③小火加热试管中的混合液;①待小试管中收集到约4mL产物时停止加热,撤出小试管并用力振荡,然后静置待其分层;⑤分离出纯净的乙酸乙酯。
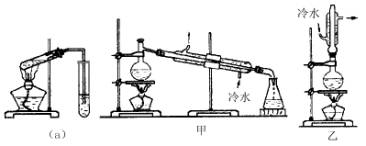
请回答下列问题:
(1)步骤①中,配制这一比例的混合液的操作是___________________。
(2)写出该反应的化学方程式________,浓H2SO4的作用是________。
(3)步骤③中,用小火加热试管中的混合液,其原因是________。
(4)步骤④所观察到的现象是________,写出原因与结论:________。
(5)步骤⑤中,分离出乙酸乙酯选用的仪器是________,产物应从________口倒出,因为________。
(6)为提高乙酸乙酯的产率,甲、乙两位同学分别设计了如上图甲、乙的装置(乙同学待反应完毕冷却后再用饱和Na2CO3溶液提取烧瓶中产物)。你认为哪种装置合理,为什么?答________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com