
题目列表(包括答案和解析)
重铬酸钾是工业生产和实验室的重要氧化剂,工业上常用铬铁矿(主要成份为FeO • Cr2O3)为原料生产,实验室模拟工业法用铬铁矿制K2Cr2O7的主要工艺如下,涉及的主要反应是:
6FeO·Cr2O3+24NaOH+7KClO3 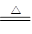 12Na2CrO4+3Fe2O3+7KCl+12H2O
12Na2CrO4+3Fe2O3+7KCl+12H2O

请回答下列问题:
(1)在反应器①中,有Na2CrO4生成,同时Fe2O3转变为NaFeO2,杂质SiO2、Ai2O3与纯碱反应转变为可溶性盐,写出氧化铝与碳酸钠反应的化学方程式:________________。
(2) NaFeO2能强烈水解,在操作②生成沉淀而除去,写出该反应的化学方程式: _______________。
(3)简要叙述操作③的目的:________________________。
(4)操作④中,酸化时,CrO42-转化为Cr2O72-,写出平衡转化的离子方程式:___________。
(5)称取重铬酸钾试样2. 5000g配成250mL溶液,取出25.00mL于碘量瓶中,加 入10 mL 2mol/L H2SO4和足量碘化钾(铬的还原产物为Cr3+),放于暗处5min,然后加入100mL水,加入3mL淀粉指示剂,用0.1200mol/LNa2S2O3标准溶液滴定(I2+2S2O32-=2I-+S4O62-),若刚达到滴定终点共用去Na2S2O3标准溶液40.00mL,则所得产品重铬酸钾的纯度________________ (设整个过程中其它杂质不参与反应)。
| A.分别向盛有5mL0.1mol?L-1Na2CO3溶液、NaHCO3溶液的试管中加入3mL0.1mol?L-1盐酸,后者放出CO2气体快 |
| B.25℃时,一份双氧水样品经过2h,H2O2的浓度从5×10-2mol?L-1下降到3×10-2mol?L-1,该双氧水在这2h中分解的平均速率约是1.67×10-4mol?(L?min)-1 |
| C.用含硫矿石(如黄铁矿)燃烧制二氧化硫气体时,为了增大二氧化硫的生成速率,常将矿石粉碎成颗粒状、在沸腾炉内鼓入强大空气流,把矿石吹得剧烈翻腾 |
| D.H2能在O2中安静地燃烧,点燃H2和空气的混合气体可能会发生爆炸,前者是因为纯净的O2和H2反应较慢,后者是因为空气中含有大量的N2能促进H2的燃烧 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com