
题目列表(包括答案和解析)
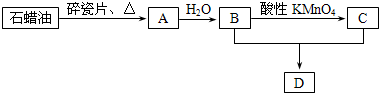
| Cu |
| △ |
| Cu |
| △ |
| 浓硫酸 |
| △ |
| 浓硫酸 |
| △ |

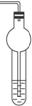
操作步骤:(1)如图装置Ⅰ所示,组装好实验装置。
(2)加入乙醇、乙酸及浓硫酸,点燃酒精灯缓慢加热。
(3)将产生的蒸气经导管导入装置A中,观察现象。
回答下列问题:
(1)请写出该反应的反应方程式:____________________。
(2)某同学在做实验时,为防止倒吸,对A装置进行的改进,请在右边虚框中画出改进部分装置图。
(3)若该同学用
①反应过程中升温过快过高,从而使一部分反应物未来得及充分反应
②该反应为可逆反应,反应不能进行彻底
③生成的乙酸乙酯未能充分冷凝下来
(4)为了提高反应物的利用率,另一同学认为采用了装置Ⅱ,你认为有何优点?__________________。
(8分)某有机物A只含有C、H、O三种元素,常用作有机合成的中间体。现将8.4 g该有机物在13.44L(标况下)O2经充分燃烧后将产生的热气体(无有机物)先通过足量的CuSO4固体,发现该固体增重7.2g,然后再将该剩余气体通入足量的澄清石灰水,石灰水增重17.6 g;质谱图表明其相对分子质量为84,红外光谱分析表明A分子中含有O—H键和位于分子端的C≡C键,核磁共振氢谱有三个峰,峰面积为6:1:1。
(1)通过计算确定该有机物A的分子式,并写出A的结构简式(要有计算过程)。
(2)有机物B是A的同分异构体,1 mol B可与1mol Br2加成。该有机物所有碳原子在同一个平面,没有顺反异构现象。请写出B的结构简式是。
(17分)某同学利用下图所示的实验装置进行铁跟水蒸气反应的实验,并继续研究铁及其化合物的部分性质。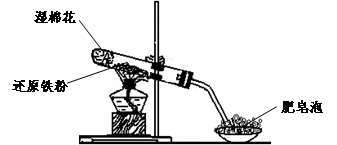
已知:①FeO + 2H+ = Fe2+ + H2O②Fe2O3 + 6H+ = 2Fe3+ +3 H2O ③Fe3O4 + 8H+ = Fe2+ +2Fe3+ +4 H2O
请回答下列问题:
(1)硬质试管中发生反应的化学方程式为 。
(2)该同学欲确定反应一段时间后硬质试管中固体物质的成分,设计了如下实验方案:
①待硬质试管冷却后,取少许其中的固体物质溶于稀硫酸得溶液B;
②取少量溶液B滴加KSCN溶液,若溶液变红色则说明硬质试管中固体物质的成分是(只有一个选项符合题意) ,若溶液未变红色则说明硬质试管中固体物质的成分是(只有一个选项符合题意) 。
| A.一定有Fe3O4,可能有Fe | B.只有Fe(OH)3 | C.一定有Fe3O4和Fe |
| D.一定有Fe(OH)3,可能有Fe E.只有Fe3O4 |


(8分)某有机物A只含有C、H、O三种元素,常用作有机合成的中间体。现将8.4 g该有机物在13.44L(标况下)O2经充分燃烧后将产生的热气体(无有机物)先通过足量的CuSO4固体,发现该固体增重7.2g,然后再将该剩余气体通入足量的澄清石灰水,石灰水增重17.6 g;质谱图表明其相对分子质量为84,红外光谱分析表明A分子中含有O—H键和位于分子端的C≡C键,核磁共振氢谱有三个峰,峰面积为6:1:1。
(1)通过计算确定该有机物A的分子式,并写出A的结构简式(要有计算过程)。
(2)有机物B是A的同分异构体,1 mol B可与1mol Br2加成。该有机物所有碳原子在同一个平面,没有顺反异构现象。请写出B的结构简式是。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com