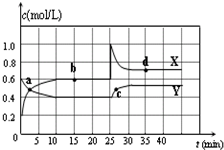
I.在恒温条件下将一定量X和Y的混合气体通入一容积为2L的密闭容器中,
X和Y两物质的浓度随时间变化情况如图.
(1)该反应的化学方程式为(反应物或生成物用符号X、Y表示):
Y
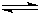
2X
Y
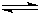
2X
.
(2)a、b、c、d四个点中,表示化学反应处于平衡状态的点是
b、d
b、d
.
II.如图是可逆反应X
2+3Y
2 
2Z
2 在反应过程中的反应速率(?)与时间(t)的关系曲线,下列叙述正确的是
B、D
B、D
.
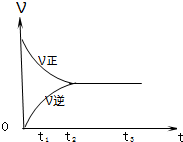
A、t
1时,只有正方向反应
B、t
2时,反应到达限度
C、t
2-t
3,反应不再发生
D、t
2-t
3,各物质的浓度不再发生变化
III.以下是关于化学反应2SO
2+O
2 
2SO
3 的两个素材:
素材1:某温度和压强下,2升容器中,不同时间点测得密闭体系中三种物质的物质的量
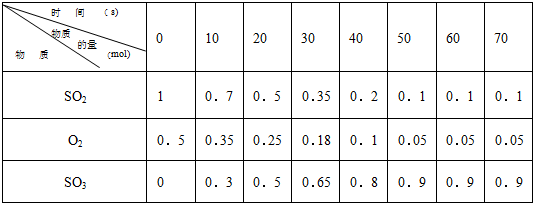
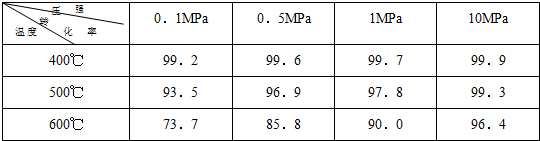
素材2:在不同条件下进行时测得SO
2的转化率:(SO
2的转化率是反应的SO
2占起始SO
2的百分数)
从以上的两个素材中体会:
(1)根据素材1中计算20-30s期间,用二氧化硫表示的化学反应的平均速率为:
0.0075mol?L-1?s-1
0.0075mol?L-1?s-1
.
(2)根据素材2中分析得到,提高该化学反应限度的途径有:
增大压强或在一定范围内降低温度
增大压强或在一定范围内降低温度
.
(3)根据素材1、素材2中分析得到,要实现素材1中SO
2的转化率需控制的反应条件是
温度为600℃,压强为1MPa
温度为600℃,压强为1MPa
.


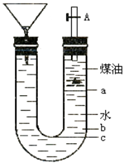 用如图的实验装置可以进行钠跟水的反应实验,并可收集、检验生成的气体.Na的密度为0.97g/mL,煤油的密度为0.87g/mL,请回答下列问题:
用如图的实验装置可以进行钠跟水的反应实验,并可收集、检验生成的气体.Na的密度为0.97g/mL,煤油的密度为0.87g/mL,请回答下列问题: I.在恒温条件下将一定量X和Y的混合气体通入一容积为2L的密闭容器中,
I.在恒温条件下将一定量X和Y的混合气体通入一容积为2L的密闭容器中,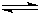 2X
2X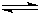 2X
2X 2Z2 在反应过程中的反应速率(?)与时间(t)的关系曲线,下列叙述正确的是
2Z2 在反应过程中的反应速率(?)与时间(t)的关系曲线,下列叙述正确的是
 2SO3 的两个素材:
2SO3 的两个素材:
