
题目列表(包括答案和解析)
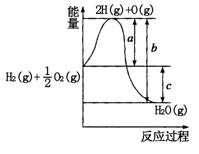
(10分)已知:H2(g)+O2(g)=H2O(g),反应过程中能量变化如图所示: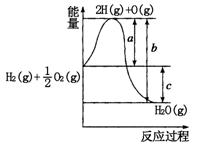
请回答下列问题:
(1)a、b、c分别代表的意义
a. ,
b. ,
c. ;
(2)该反应是 反应(填“放热”或“吸热”),ΔH 0(填“>”、“<”或“=”);
(3)若已知2H2 (g)+O2(g)=2H2O(g) ΔH1=-Q1kJ·mol-1;
2H2 (g)+O2(g)=2H2O(l) ΔH2=-Q2kJ·mol-1,
则ΔH1 ΔH2,Q1 Q2(填“>”“<”或“=”)。
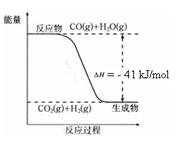
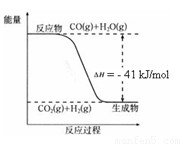
已知工业制氢气的反应为CO(g) + H2O(g) ![]() CO2(g) + H2(g),反应过程中能量变化如右图所示。在500 ℃时的平衡常数 K = 9。若在2 L的密闭容器中CO和水蒸气的起始浓度都是0.1 mol/L,10 min时达到平衡状态。
CO2(g) + H2(g),反应过程中能量变化如右图所示。在500 ℃时的平衡常数 K = 9。若在2 L的密闭容器中CO和水蒸气的起始浓度都是0.1 mol/L,10 min时达到平衡状态。
(1)增加H2O(g)的浓度,CO的转化率将 (填“增大”“减小”或“不变”)。
(2)平衡常数的表达式K = 。400 ℃时的平衡常数K 9(填“>”“<”或”“=”)。
(3)500 ℃时,10 min内v(H2O)= ,在此过程中体系的能量将 (填“增加”或“减少”) kJ。
(4)已知 2H2 (g) + O2 (g) = 2H2O (g) ΔH=-484 kJ/mol
结合上图写出CO完全燃烧生成CO2的热化学方程式: 。
已知工业制氢气的反应为CO(g) + H2O(g)  CO2(g) + H2(g),反应过程中能量变化如右图所示。在500 ℃时的平衡常数 K = 9。若在2 L的密闭容器中CO和水蒸气的起始浓度都是0.1 mol/L,10 min时达到平衡状态。
CO2(g) + H2(g),反应过程中能量变化如右图所示。在500 ℃时的平衡常数 K = 9。若在2 L的密闭容器中CO和水蒸气的起始浓度都是0.1 mol/L,10 min时达到平衡状态。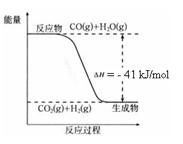
(1)增加H2O(g)的浓度,CO的转化率将 (填“增大”“减小”或“不变”)。
(2)平衡常数的表达式K = 。400 ℃时的平衡常数K 9(填“>”“<”或”“=”)。
(3)500 ℃时,10 min内v(H2O)= ,在此过程中体系的能量将 (填“增加”或“减少”) kJ。
(4)已知 2H2 (g) + O2 (g) = 2H2O (g) ΔH=-484 kJ/mol
结合上图写出CO完全燃烧生成CO2的热化学方程式: 。
已知工业制氢气的反应为CO(g) + H2O(g)  CO2(g) + H2(g),反应过程中能量变化如右图所示。在500 ℃时的平衡常数 K = 9。若在2
L的密闭容器中CO和水蒸气的起始浓度都是0.1 mol/L,10 min时达到平衡状态。
CO2(g) + H2(g),反应过程中能量变化如右图所示。在500 ℃时的平衡常数 K = 9。若在2
L的密闭容器中CO和水蒸气的起始浓度都是0.1 mol/L,10 min时达到平衡状态。
(1)增加H2O(g)的浓度,CO的转化率将 (填“增大”“减小”或“不变”)。
(2)平衡常数的表达式K = 。400 ℃时的平衡常数K 9(填“>”“<”或”“=”)。
(3)500 ℃时,10 min内v(H2O)= ,在此过程中体系的能量将 (填“增加”或“减少”) kJ。
(4)已知 2H2 (g) + O2 (g) = 2H2O (g) ΔH=-484 kJ/mol
结合上图写出CO完全燃烧生成CO2的热化学方程式: 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com