
题目列表(包括答案和解析)
可逆反应:![]() 在温度T1、T2,压强Pl、P2下,产物D的物质的量n与反应时间t的关系如右图所示。下述各项中不正确的是
在温度T1、T2,压强Pl、P2下,产物D的物质的量n与反应时间t的关系如右图所示。下述各项中不正确的是
A.T1< T2 B.Pl<P2
C.正反应为放热反应 D.m+n<p+q
有可逆反应A+B![]() 2C在不同温度下经过一定时间,
2C在不同温度下经过一定时间,
混合物中C的百分含量与温度关系如右图所示,那么:
(1)反应在___________________温度下达到化学平衡;
(2)此正反应为______________________热反应;
(3)由T1向T2变化时,V正____________V逆(填>、<、=);
(4)由T3向T4变化时,V正_____________V逆(填>、<、=).


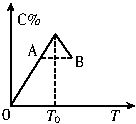
对于可逆反应2A+B 2C,在反应过程中C的物质的量分数随温度变化如右图所示。则:
2C,在反应过程中C的物质的量分数随温度变化如右图所示。则:
(1)T0对应的v正与v逆的关系是________。
(2)正反应为________热反应。
(3)A、B两点正反应速率的大小关系是_______。
(4)温度T<T0时,C%逐渐增大的原因是______。
 已知反应:CO(g)+H2O(g)?H2(g)+CO2(g)△H=-41.2kJ/mol,生成的CO2与H2以不同的体积比混合时在合适条件下的反应可制得CH4.
已知反应:CO(g)+H2O(g)?H2(g)+CO2(g)△H=-41.2kJ/mol,生成的CO2与H2以不同的体积比混合时在合适条件下的反应可制得CH4.| 1 | 2 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com