
题目列表(包括答案和解析)
| A、CO(g)+2H2(g)═CH3OH(g)△H>-90.5kJ?mol-1 | ||
| B、在甲醇燃料电池中,甲醇所在电极为正极 | ||
C、CH4(g)+
| ||
D、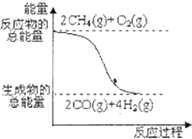 反应①中的能量变化如图所示 |
| A、甲烷的燃烧热△H=-890kJ/mol | B、当4NA个碳氧共用电子对生成时,反应③放出890kJ的能量 | C、甲醇的燃烧热△H=-1528 kJ/mol | D、若CO的燃烧热△H=-282.5 kJ/mol,则H2的燃烧热△H=-286 kJ/mol |
甲醇广泛用作燃料电池的燃料,可用天然气来合成,已知:
|
②CO(g)+2H2(g)=CH3OH(l) ; △H=-90.5kJ·mol-1
下列描述错误的是( )
A.CO(g)+2H2(g)==CH3OH(g)
△H>-90.5kJ·mol-1
B.在甲醇燃料电池中,甲醇所在电极为正极
C.CH4(g)+1/2o2(g)===CH3(OH)(l)
△H=-126kJ·mol-1
D.反应①中的能量变化如右图所示
甲醇广泛用作燃料电池的燃料,可用天然气来合成,已知:
|
②CO(g)+2H2(g)=CH3OH(l); △H=-90.5kJ·mol-1
下列描述错误的是( )
A.CO(g)+2H2(g)==CH3OH(g)
△H>-90.5kJ·mol-1
B.在甲醇燃料电池中,甲醇所在电极为正极
C.CH4(g)+1/2o2(g)===CH3(OH)(l)
△H=-126kJ·mol-1
D.反应①中的能量变化如右图所示
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com