
题目列表(包括答案和解析)
pH=5的盐酸和pH=5的氯化铵溶液,两溶液中水电离出的氢离子浓度依次为xmol/L和ymol/L,则它们的关系是
[ ]
A.相等
B.x>y

 pC类似pH,是指极稀溶液中溶质物质的量浓度的常用对数负值,如溶液中某溶质的浓度为:1×10-3mol·L-1,则pC=-lg(1×10-3)=3。H2CO3溶液的pC-pH关系如图。
pC类似pH,是指极稀溶液中溶质物质的量浓度的常用对数负值,如溶液中某溶质的浓度为:1×10-3mol·L-1,则pC=-lg(1×10-3)=3。H2CO3溶液的pC-pH关系如图。
请回答下列问题:
(1)pH=2~4时,H2CO3溶液中主要存在的离子为 。
(2)已知碳酸溶液中存在平衡:H2O+CO2 H2CO3
H2CO3![]() H++HCO3-。当溶液pH由5减小到0时,溶液中H2CO3的pC基本不变的原因是
H++HCO3-。当溶液pH由5减小到0时,溶液中H2CO3的pC基本不变的原因是
。
(3)能够抵抗外来少量酸碱的影响、保持自身 pH变化不大的溶液,称之为缓冲溶液。如浓度均为0.1mol·L-1的NaHCO3和Na2CO3混合溶液就是一种缓冲溶液,加入少量酸或碱,由于平衡HCO3- H++CO32-移动,溶液中H+浓度变化不大。根据上述信息,下列不能形成缓冲溶液的是 。
H++CO32-移动,溶液中H+浓度变化不大。根据上述信息,下列不能形成缓冲溶液的是 。
A.碳酸钠和氢氧化钠的混和溶液 B.醋酸和醋酸钠的混和溶液
C.硫酸和硫酸钠的混合溶液 D.氨水和氯化铵的混和溶液
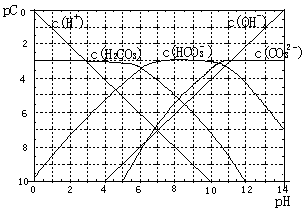 pC类似pH,是指极稀溶液中溶质物质的量浓度的常用对数负值,如溶液中某溶质的浓度为:1×10-3mol·L-1,则pC=-lg(1×10-3)=3。H2CO3溶液的pC-pH关系如图。
pC类似pH,是指极稀溶液中溶质物质的量浓度的常用对数负值,如溶液中某溶质的浓度为:1×10-3mol·L-1,则pC=-lg(1×10-3)=3。H2CO3溶液的pC-pH关系如图。
请回答下列问题:
(1)pH=2~4时,H2CO3溶液中主要存在的离子为 。
(2)已知碳酸溶液中存在平衡:H2O+CO2 H2CO3
H2CO3 H++HCO3-。当溶液pH由5减小到0时,溶液中H2CO3的pC基本不变的原因是
H++HCO3-。当溶液pH由5减小到0时,溶液中H2CO3的pC基本不变的原因是
。
(3)能够抵抗外来少量酸碱的影响、保持自身 pH变化不大的溶液,称之为缓冲溶液。如浓度均为0.1mol·L-1的NaHCO3和Na2CO3混合溶液就是一种缓冲溶液,加入少量酸或碱,由于平衡HCO3- H++CO32-移动,溶液中H+浓度变化不大。根据上述信息,下列不能形成缓冲溶液的是
。
H++CO32-移动,溶液中H+浓度变化不大。根据上述信息,下列不能形成缓冲溶液的是
。
A.碳酸钠和氢氧化钠的混和溶液 B.醋酸和醋酸钠的混和溶液
C.硫酸和硫酸钠的混合溶液 D.氨水和氯化铵的混和溶液
(8分)Ⅰ.(1)饱和氯化铵溶液显酸性,原因是
________________________________________________________________________
________________________________________________________________________;
向饱和氯化铵溶液中加入少量Mg(OH)2固体,固体完全溶解;其合理的解释(用相关离子方程式表示)为
________________________________________________________________________
________________________________________________________________________。
(2)向Mg(OH)2悬浊液中加入适量CH3COONH4溶液,
Mg(OH)2能否完全溶解________(填“能”或“否”),理由是
________________________________________________________________________
________________________________________________________________________。
Ⅱ.硫酸是强酸,中学阶段将硫酸在水溶液中看作完全电离。但事实是,硫酸在水中的第一步电离是完全的,第二步电离并不完全,其电离情况为:H2SO4===H++HSO4-,HSO4-===H++SO42-。
请回答下列有关问题:
(1)Na2SO4溶液呈________(填“弱酸性”“中性”或“弱碱性”),其理由是________________________________________________________________________
(用离子方程式表示);
(2)H2SO4溶液与BaCl2溶液反应的离子方程式为
________________________________________________________________________
________________________________________________________________________。
(3)在0.10 mol·L-1的Na2SO4溶液中,下列离子浓度关系正确的是________(填写编号);
A.c(Na+)=c(SO42-)+c(HSO4-)+c(H2SO4)
B.c(OH-)=c(HSO4-)+c(H+)
C.c(Na+)+c(H+)=c(OH-)+c(HSO4-)+2c(SO42-)
D.c(Na+)=2c(SO42-)+2c(HSO4-)
(4)写出NaHSO4溶液中溶质电离常数(Ka)的表达式________________;
(5)若25℃时,0.10 mol·L-1的NaHSO4溶液中c(SO2-4)=0.029 mol·L-1,则0.10 mol·L-1的H2SO4溶液中c(SO42-)________0.029mol·L-1(填“<”“>”或“=”),其理由是________________________________________________________________________;
(6)如果25℃时,0.10 mol·L-1H2SO4溶液的pH=
-lg 0.11,则0.10 mol·L-1的H2SO4溶液中c(SO42-)=________mol·L-1。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com