Ⅰ.实验室使用容量瓶来配制一定体积、一定浓度的溶液.现在实验室需要0.10mol?L
-1NaOH溶液450mL,根据溶液配制中的情况回答下列问题:
(1)实验中除了托盘天平(带砝码)、烧杯、玻璃棒、胶头滴管、药匙外,还需要的仪器有
500mL容量瓶
500mL容量瓶
.
(2)根据计算得知,需称取NaOH固体的质量为
2.0
2.0
g.
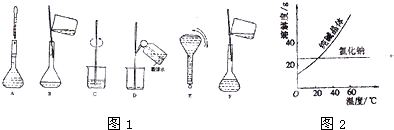
(3)配制过程中有几个关键的步骤和操作如图1所示,将实验步骤A-F按实验过程先后次序排列
CBDFAE
CBDFAE
.
(4)配制一定物质的量浓度溶液的实验中,下列操作会导致溶液浓度偏高的是
B
B
.
A.在托盘天平的两托盘中分别放等质量的纸,称取NaOH固体
B.将NaOH固体在烧杯中溶解后迅速小心转移至容量瓶中
C.定容时不小心加水超过了刻度线,此时迅速用胶头滴管吸出一些
D.定容时仰视容量瓶刻度线
Ⅱ.阅读、分析下列两个材料:
材料一:如图2
材料二:
| 物质 |
熔点/℃ |
沸点/℃ |
密度/g?cm-3 |
溶解性 |
乙二醇C2H6O2 |
-11.5 |
198 |
1.11 |
易溶于水和乙醇 |
丙三醇C3H8O3 |
17.9 |
290 |
1.26 |
能跟水、酒精以任意比互溶 |
根据上述材料及课本知识,回答下列问题(填写序号):
A.蒸馏法B.萃取法C.“溶解、结晶、过滤”的方法D.分液法
(1)将纯碱从氯化钠和纯碱的混合物中分离出来,最好应用
C
C
;
(2)将乙二醇和丙三醇相互分离的最佳方法是
A
A
.
Ⅲ.有一固体粉末,其中可能含有Na
2CO
3、NaCl、Na
2SO
4、CuCl
2、Ba(NO
3)
2、K
2CO
3中的一种或几种,现按下列步骤进行实验.
(1)将该粉末溶于水得无色溶液和白色沉淀.
(2)在滤出的沉淀中加入稀硝酸,有部分沉淀溶解,同时产生无色气体.
(3)取滤液做焰色反应,火焰呈黄色,透过蓝色的钴玻璃观察,未见火焰呈紫色.由上述现象推断:该混合物中一定含有
Na2CO3、Na2SO4、Ba(NO3)2
Na2CO3、Na2SO4、Ba(NO3)2
;一定不含有
CuCl2、K2CO3
CuCl2、K2CO3
;可能含有
NaCl
NaCl
.