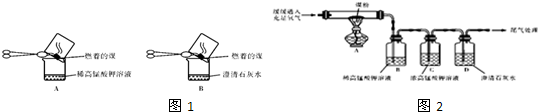
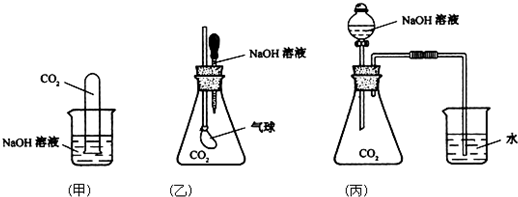
甲、乙、丙三位同学分别用如下实验装置及化学药品(碱石灰为氢氧化钠和生石灰的混合物)制取氨气.请你参与探究,并回答问题:
(1)制取氨气的化学方程式为:
2NH4Cl+Ca(OH)2═CaCl2+2NH3↑+2H2O
2NH4Cl+Ca(OH)2═CaCl2+2NH3↑+2H2O
;
(2)三位同学都用向下排空气法收集氨气,其原因是
氨气的密度比空气小,氨气极易溶于水
氨气的密度比空气小,氨气极易溶于水
;
(3)三位同学用上述装置制取氨气时,其中有一位同学没有收集到氨(实验操作都正确),你认为没有收集到氨气的同学是
乙
乙
填(“甲”、“乙”或“丙”);
(4)检验氨气是否收集满的方法是(简述操作方法、现象和结论):
用湿润的红色石蕊试纸靠近试管口,如果试纸变蓝,则氨气已满
用湿润的红色石蕊试纸靠近试管口,如果试纸变蓝,则氨气已满
.
(5)三位同学都认为,采用上述各自的装置,还可用于加热碳酸氢铵固体的方法来制取纯净的氨气,你认为那位同学能够达到实验目的
丙
丙
(填“甲”、“乙”或“丙”).他们还认为,装置中的NH
4HCO
3固体可用NH
4Cl固体代替,你认为
不能
不能
(填“能”或“不能”).
(6)某课外活动小组查阅有关资料知,铂丝是氨氧化的催化剂.并设计进行了如图实验.实验过程中观察到:瓶口气体变为红棕色,瓶内出现白烟
写出此实验过程中化学反应方程式:
;
2NO+O2═2NO2
2NO+O2═2NO2
;
3NO2+H2O═2HNO3+NO
3NO2+H2O═2HNO3+NO
;
NH3+HNO3═NH4NO3
NH3+HNO3═NH4NO3
.