
题目列表(包括答案和解析)
高锰酸钾是一种重要的化学试剂,其溶液不很稳定,在酸性条件下会分解生成二氧化锰和氧气,在中性或弱碱性溶液中分解速度很慢,见光分解速度加快。
(1)酸性条件下高锰酸钾溶液分解的离子方程式 。
(2)请配平高锰酸钾溶液与草酸钠Na2C2O4溶液在酸性条件下反应的离子方程式:
______MnO4— +______C2O42—+______H+=______Mn2++______CO2↑+____________
(3)某学习小组为了探究高锰酸钾溶液和草酸钠溶液的反应过程,将高锰酸钾溶液逐滴地滴入一定体积的酸性草酸钠溶液中(温度相同,并不断振荡时),记录的现象如下表:
滴入高锰酸钾溶液的次序(每滴溶液的体积相同) |
高锰酸钾溶液紫色褪去的时间 |
|
先滴入第1滴 |
1min |
|
褪色后再滴入第2滴 |
15s |
|
褪色后再滴入第3滴 |
3s |
|
褪色后再滴入第4滴 |
1s |
请分析高锰酸钾溶液褪色时间变化的原因 。
(4)该学习小组在获取了上述经验和结论以后,用稳定的物质草酸钠Na2C2O4(相对分子质量134.0)来标定高锰酸钾溶液的浓度。他们准确称取1.340g纯净的草酸钠配成250mL溶液,每次准确量取25.00mL溶液酸化后用KMnO4溶液滴定。
①高锰酸钾溶液应装在 (填下图中的仪器编号)。
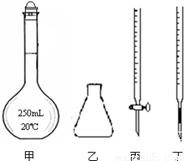
②为了防止高锰酸钾在酸性条件下分解而造成误差,滴定时应注意的是 。
③若在实验过程中存在下列操作,其中会使所测KMnO4浓度偏低的是 。
A.未润洗盛放KMnO4的滴定管
B.滴定前尖嘴部分无气泡,滴定终点时出现气泡
C.定容时,俯视刻度线
D.锥形瓶用水洗之后未用待测液润洗
④当溶液呈微红色且半分钟内不褪色,消耗KMnO4溶液20.00mL(多次测定的平均值),则KMnO4溶液的浓度为 。


处理含CO、SO2烟道气污染的一种方法,是将其在催化剂作用下转化为单质S(g)。发生反应为:2CO(g)+SO2(g) ![]() S(g)+2CO2(g)
S(g)+2CO2(g)
(1)已知:CO(g)+![]() O2(g)=CO2(g) △H=-283.0kJ·mol—1
O2(g)=CO2(g) △H=-283.0kJ·mol—1
S(g)+O2(g)=SO2(g) △H= - 296.0 kJ·mol—1
试写出利用上述方法处理烟道气的热化学方程式
(2)在容积为2L的密闭容器中,充入4molCO和2molSO2,在一定条件下发生反应2CO(g)+SO2(g) S(g)+2CO2(g),CO2的物质的量分数随时间的变化如图所示,则:
①0-2min内的平均反应速率v(CO)= 。
②该温度下,上述反应的平衡常数K= (填数值)。
③2min后改变下列条件能使上述反应的反应速率增大,且平衡向正 向移动的是
a.选用更高效的催化剂 b.升高温度 c.及时分离出二氧化碳 d.增加SO2的浓度

在容积固定的密闭容器中充入一定量的X、Y两种气体,一定条件下发生如下可逆反应并达到平衡:3X(g)+Y(g)ƒ2Z(g),DH<0,测得X的转化率为37.5%,Y的转化率为X的![]() 。下列有关叙述正确的是( )
。下列有关叙述正确的是( )
A.若测得X的反应速率为0.2mol×L-1×s-1,则Z的反应速率为0.3mol×L-1×s-1
B.充入氦气,容器压强增大,Y的转化率提高
C.开始充入容器中的X、Y物质的量比为2∶1
D.升高温度,正反应速率减小,平衡向逆反应方向移动
A.若测得X的反应速率为0.2mol×L-1×s-1,则Z的反应速率为0.3mol×L-1×s-1
B.充入氦气,容器压强增大,Y的转化率提高
C.开始充入容器中的X、Y物质的量比为2∶1
D.升高温度,正反应速率减小,平衡向逆反应方向移动
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com