
题目列表(包括答案和解析)
(14分)㈠在一定条件下的下列可逆反应达到平衡时,试填出:xA+yB![]() zC
zC
(1)若A、B、C都是气体,在减压后平衡向逆反应方向移动,则x、y、z关系是
;
(2)若C是气体,并且x+y=z,在加压时化学平衡可发生移动,则平衡必定是向
方向移动;
(3)已知B、C是气体,现增加A物质的量,平衡不移动,说明A是 (填状态);
(4) 若加热后,C的百分含量减小,则正反应是________热反应。
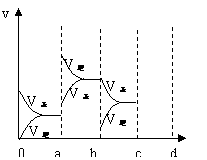 ㈡右图表示在密闭容器中反应:
㈡右图表示在密闭容器中反应:
2SO2+O2![]() 2SO3,△H <0;达到平衡时,
2SO3,△H <0;达到平衡时,
由于条件改变而引起反应速率和化学平衡的变化情况,
⑴a b过程中改变的条件可能是 ;
⑵b c过程中改变的条件可能是 ;
⑶若增大压强时,反应速率变化情况画在c—d处。
 2SO3在不同条件下进行时SO2的转化率:
2SO3在不同条件下进行时SO2的转化率:| 温度\压强 | 0.1MPa | 0.5MPa | 1MPa | 10MPa |
| 400℃ | 99.2 | 99.6 | 99.7 | 99.9 |
| 500℃ | 93.5 | 96.9 | 97.8 | 99.3 |
| 600℃ | 73.7 | 85.8 | 89.5 | 96.4 |
 2SO3,平衡时SO3为amol,在相同温度下分别按下列配比在VL密闭容器中放入起始物质,平衡时有关SO3的物质的量叙述正确的是( )。
2SO3,平衡时SO3为amol,在相同温度下分别按下列配比在VL密闭容器中放入起始物质,平衡时有关SO3的物质的量叙述正确的是( )。 2SO3,平衡时SO3为a mol,在相同温度下分别按下列配比在V L密闭容器中放入起始物质,平衡时有关SO3的物质的量叙述正确的是
2SO3,平衡时SO3为a mol,在相同温度下分别按下列配比在V L密闭容器中放入起始物质,平衡时有关SO3的物质的量叙述正确的是A.放入0.3 mol SO2、0.1 mol O2、0.1 mol SO3,达到平衡时SO3必小于a mol
B.放入0.2 mol SO2、0.1 mol O2、0.2 mol SO3,达到平衡时SO3必大于a mol
C.放入0.4 mol SO2、0.1 mol O2,达到平衡时SO3必等于0.4 mol
D.放入0.2 mol SO2、0.1 mol O2,达到平衡时SO3必小于a mol
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com