
题目列表(包括答案和解析)
| M | N | |
| 第一电离能(kJ/mol) | 495.8 | 418.8 |





| 4×99.5g/mol |
| ag/cm3×6.02×1023mol-1 |
| 4×99.5g/mol |
| ag/cm3×6.02×1023mol-1 |
有4种物质的量浓度相同且由一价阳离子A+、B+和一价阴离子X-、Y-组成的盐溶液,据测试,常温下AX溶液和BY溶液的pH都为7,AY溶液的pH大于7,BX溶液的pH小于7。据此推知其中可能不水解的盐是()
A.AXB.BXC.AYD.BY
[选修一物质结构与性质] (15分)
有X、Y、Z、Q、M 、E、N、G前四周期且原子序数递增的八种元素,其中X的原子中没有成对电子,Y元素基态原子中电子占据三种能量不同的原子轨道且每种轨道中的电子数相同,Z元素基态原子核外有两个电子层,最外层有3个未成对电子,Q的基态原子核外成对电子数是成单电子数的3倍,E原子得到一个电子后3p轨道全充满,G+中所有电子正好全部充满K、L、M三个电子层。M、N原子的价层电子构型为nS1,其电离能数据如下表:
|
| M | N |
| 第一电离能(kJ/mol) | 495.8 | 418.8 |
回答下列问题:
(1)Z元素原子的价层电子的轨道表示式为: ;
(2)由X、Y形成的Y2X2分子中,含有 个键, 个
键:
(3)比较ME、NE的熔点高低并说明理由 。
(4)Y、Z、Q的第一电离能由小到大的顺序为 。(用元素符号回答)
(5)YQ2中心原子的杂化方式为___________,有一种与YQ2互为等电子体的离子,能用于鉴别Fe3+ ,写出其电子式________________。
(6)GE的晶胞结构如图所示,阴离子周围最近的阳离子有 个;GE晶体的密度为ag·cm-3,则晶胞的体积是 (只要求列出计算式)。
[选修一物质结构与性质] (15分)
有X、Y、Z、Q、M 、E、N、G前四周期且原子序数递增的八种元素,其中X的原子中没有成对电子,Y元素基态原子中电子占据三种能量不同的原子轨道且每种轨道中的电子数相同,Z元素基态原子核外有两个电子层,最外层有3个未成对电子,Q的基态原子核外成对电子数是成单电子数的3倍,E原子得到一个电子后3p轨道全充满,G+中所有电子正好全部充满K、L、M三个电子层。M、N原子的价层电子构型为nS1,其电离能数据如下表:
| | M | N |
| 第一电离能(kJ/mol) | 495.8 | 418.8 |
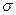 键, 个
键, 个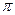 键:
键: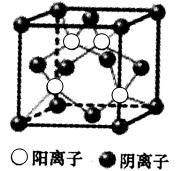
[选修一物质结构与性质] (15分)
有X、Y、Z、Q、M 、E、N、G前四周期且原子序数递增的八种元素,其中X的原子中没有成对电子,Y元素基态原子中电子占据三种能量不同的原子轨道且每种轨道中的电子数相同,Z元素基态原子核外有两个电子层,最外层有3个未成对电子,Q的基态原子核外成对电子数是成单电子数的3倍,E原子得到一个电子后3p轨道全充满,G+中所有电子正好全部充满K、L、M三个电子层。M、N原子的价层电子构型为nS1,其电离能数据如下表:
|
|
M |
N |
|
第一电离能(kJ/mol) |
495.8 |
418.8 |
回答下列问题:
(1)Z元素原子的价层电子的轨道表示式为: ;
(2)由X、Y形成的Y2X2分子中,含有 个 键, 个
键, 个 键:
键:
(3)比较ME、NE的熔点高低并说明理由 。
(4)Y、Z、Q的第一电离能由小到大的顺序为 。(用元素符号回答)
(5)YQ2中心原子的杂化方式为___________,有一种与YQ2互为等电子体的离子,能用于鉴别Fe3+ ,写出其电子式________________。
(6)GE的晶胞结构如图所示,阴离子周围最近的阳离子有 个;GE晶体的密度为ag·cm-3,则晶胞的体积是 (只要求列出计算式)。

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com