某化学兴趣小组的同学在学习了《铝 金属材料》一节后,产生了浓厚的实验探究兴趣,欲对氢氧化铝的化学性质进行实验探究。请你帮助他们完成实验方案和记录并回答有关的问题。
实验目的
1.观察氢氧化铝与酸、碱的反应,认识氢氧化铝的特性。
2.提高实验能力,增强探究意识。
实验原理
Al(OH)
3+3H
+=Al
3++3H
2O
Al(OH)
3+OH
-=[Al(OH)
4]
-实验药品和仪器
1mol?L
-1 Al
2(SO
4)
3溶液、10%NaOH溶液、浓氨水、稀盐酸、试管、胶头滴管
实验探究
1.在一支盛有l mol?L
-1Al
2(SO
4)
3溶液的大试管中逐滴加入浓氨水,直到产生大量沉淀。
2.将上述沉淀分为三份盛在三个试管中,分别进行如下实验:
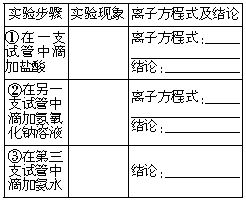
实验结论
1.通过实验探究,综合上述实验步骤①、②、③中的实验结论,你认为氢氧化铝具有___________,且氢氧化铝___________。
2.制取氢氧化铝时,用_________好。
讨论与思考
请你写出硫酸铝溶液与适量或过量氢氧化钠溶液反应时的化学方程式:______________________;________________________。
画出物质之间的物质的量的关系图:

拓展思考:查阅资料,试解释氢氧化铝为什么既能溶解在强酸溶液中,又能溶解在强碱溶液中,属于两性氢氧化物?


