ЈЁ2013?ХгҪӯЈ©АыУГ·ПҫЙРҝМъЖӨЦЖұёҙЕРФFe
3O
4ҪәМеБЈЧУј°ёұІъОпZnOЈ®ЦЖұёБчіМНјИзПВЈә

ТСЦӘЈәZnј°»ҜәПОпөДРФЦКУлAlј°»ҜәПОпөДРФЦКПаЛЖЈ®Зл»ШҙрПВБРОКМвЈә
ЈЁ1Ј©УГNaOHИЬТәҙҰАн·ПҫЙРҝМъЖӨөДЧчУГУР
AB
AB
Ј®
AЈ®ИҘіэУНОЫ BЈ®ИЬҪв¶ЖРҝІг CЈ®ИҘіэМъРв DЈ®¶Ы»Ҝ
ЈЁ2Ј©өчҪЪИЬТәAөДpHҝЙІъЙъZnЈЁOHЈ©
2іБөнЈ¬ОӘЦЖөГZnOЈ¬әуРшІЩЧчІҪЦиКЗ
ійВЛЎўПҙөУЎўЧЖЙХ
ійВЛЎўПҙөУЎўЧЖЙХ
Ј®
ЈЁ3Ј©УЙИЬТәBЦЖөГFe
3O
4ҪәМеБЈЧУөД№эіМЦРЈ¬РліЦРшНЁИлN
2Ј¬ФӯТтКЗ
ФЪN2Жш·ХПВЈ¬·АЦ№Fe2+ұ»Сх»Ҝ
ФЪN2Жш·ХПВЈ¬·АЦ№Fe2+ұ»Сх»Ҝ
Ј®
ЈЁ4Ј©Fe
3O
4ҪәМеБЈЧУДЬ·сУГјхС№№эВЛ·ўКөПЦ№МТә·ЦАлЈҝ
І»ДЬ
І»ДЬ
ЈЁМоЎ°ДЬЎұ»тЎ°І»ДЬЎұЈ©Ј¬АнУЙКЗ
ҪәМеБЈЧУМ«РЎЈ¬ійВЛКұИЭТЧНё№эВЛЦҪ
ҪәМеБЈЧУМ«РЎЈ¬ійВЛКұИЭТЧНё№эВЛЦҪ
Ј®
ЈЁ5Ј©УГЦШёхЛбјШ·ЁЈЁТ»ЦЦСх»Ҝ»№ФӯөО¶Ё·ЁЈ©ҝЙІв¶ЁІъОпFe
3O
4ЦРөД¶юјЫМъә¬БҝЈ®ИфРиЕдЦЖЕЁ¶ИОӘ0.01000mol?L
-1өДK
2Cr
2O
7ұкЧјИЬТә250mLЈ¬УҰЧјИ·іЖИЎ
0.7350g
0.7350g
g K
2Cr
2O
7ЈЁұЈБф4О»УРР§КэЧЦЈ¬ТСЦӘMЈЁK
2Cr
2O
7Ј©=294.0g?mol
-1Ј©Ј®
ЕдЦЖёГұкЧјИЬТәКұЈ¬ПВБРТЗЖчЦРІ»ұШТӘУГөҪөДУР
ўЫўЯ
ўЫўЯ
Ј®ЈЁУГұаәЕұнКҫЈ©Ј®
ўЩөзЧУМмЖҪ ўЪЙХұӯ ўЫБҝНІ ўЬІЈБ§°ф ўЭИЭБҝЖҝ ўЮҪәН·өО№Ь ўЯТЖТә№Ь
ЈЁ6Ј©өО¶ЁІЩЧчЦРЈ¬Из№ыөО¶ЁЗ°Ч°УРK
2Cr
2O
7ұкЧјИЬТәөДөО¶Ё№ЬјвЧмІҝ·ЦУРЖшЕЭЈ¬¶шөО¶ЁҪбКшәуЖшЕЭПыК§Ј¬ФтІв¶ЁҪб№ыҪ«
Ж«ҙу
Ж«ҙу
ЈЁМоЎ°Ж«ҙуЎұЎўЎ°Ж«РЎЎұ»тЎ°І»ұдЎұЈ©Ј®


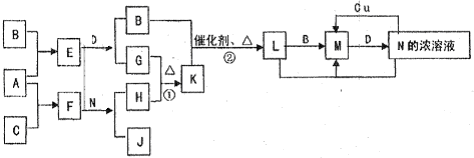
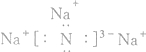
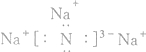
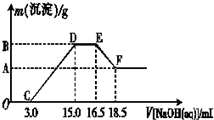 ГҫЎўВБЎўМъј°Жд»ҜәПОпФЪЙъІъәНЙъ»оЦРУР№г·әөДУҰУГЈ®
ГҫЎўВБЎўМъј°Жд»ҜәПОпФЪЙъІъәНЙъ»оЦРУР№г·әөДУҰУГЈ®