
题目列表(包括答案和解析)
| 编号 | V (Na2CO3)/mL | 沉淀情况 |
| 1 | 2.8 | 多、蓝色 |
| 2 | 2.4 | 多、蓝色 |
| 3 | 2.0 | 较多、绿色 |
| 4 | 1.6 | 较少、绿色 |
| 编号 | 反应温度/℃ | 沉淀情况 |
| 1 | 40 | 多、蓝色 |
| 2 | 60 | 少、浅绿色 |
| 3 | 75 | 较多、绿色 |
| 4 | 80 | 较多、绿色(少量褐色) |
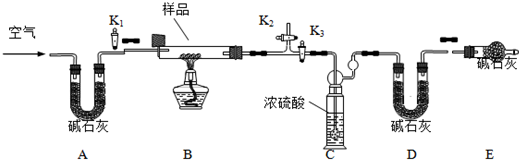
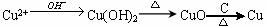
图6-4
(1)造成X河污染的主要污染源最可能分布在( )
A.ab段 B.bc段 C.cd段 D.bd段
(2)列举造成X河污染的三种可能的污染源。
(3)对c处水样进行检测,发现其中含有Cu2+等重金属离子。若要把铜离子变为单质铜回收,请完成两种回收的方法:
方法Ⅰ:_______________________________________________________________。
方法Ⅱ:______________________________________________________________。
(4)d处的污染程度比a处明显降低,请从物理学、化学、生物学三个方面简单分析其原因。
| 充电 | 放电 |
 反应A(g)+B(g)?2C(g)+D(g);△H=Q kJ/mol.过程中的能量变化如图所示,回答下列问题.
反应A(g)+B(g)?2C(g)+D(g);△H=Q kJ/mol.过程中的能量变化如图所示,回答下列问题.| c2(C)c(D) |
| c(A)c(B) |
| c2(C)c(D) |
| c(A)c(B) |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com