
题目列表(包括答案和解析)

| A.原子核外每一能层最多可容纳的电子数2n2(n为能层序数) |
| B.能层序数越大,s原子轨道的半径越大 |
| C.各能级包含的原子轨道数按s、p、d、f的顺序依次为1、3、5、7 |
| D.1个原子轨道里最多只能容纳2个电子,且自旋方向相同 |
下列说法中错误的是
| A.原子核外每一能层最多可容纳的电子数2n2(n为能层序数) |
| B.能层序数越大,s原子轨道的半径越大 |
| C.各能级包含的原子轨道数按s、p、d、f的顺序依次为1、3、5、7 |
| D.1个原子轨道里最多只能容纳2个电子,且自旋方向相同 |
A、B、C、D、E、F六种元素的原子序数依次增大。A的最高正价和最低负价的绝对值相等。B的基态原子有3个不同的能级且各能级中电子数相等。D的基态原子与B的基态原子的未成对电子数目相同,E的基态原子的s能级的电子总数与p能级的电子数相等,F的基态原子的3d轨道电子数是4s电子数的4倍。请回答下列问题:
(1)F的基态原了价电子排布式为 。
(2)B、C、D、E的原子的第一电离能由小到大的顺序为 。(用元素符号回答)
(3)下列关于B2A2分子和A2D2分子的说法正确的是
A.分子中都含有σ键和π键
B.中心原子都sp杂化
C.都是含极性键和非极性键的非极性分子
D.互为等电子体
E.B2A2分子的沸点明显低于A2D2分子
(4)F2+能与BD分子形成[F(BD)4]2+,其原因是BD分子中含有 。
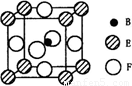
(5)由B、E、F三种元素形成的一种具有超导性的晶体,晶胞如图所示。B位于E和F原子紧密堆积所形成的空隙当中。与一个F原子距离最近的F原子的数目为 ,该晶体的化学式为 。若该晶体的相对分子质量为M,阿伏加德罗常数为NA,B、E、F三种元素的原子半径分别为r1pm、r2pm、r3pm,,则该晶体的密度表达式为 g·cm3。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com