
题目列表(包括答案和解析)
|
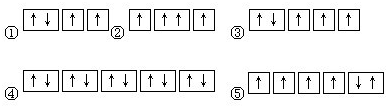
某元素基态原子的电子排布式为1s22s22p63s23p1,此元素最可能的价态是 | |
| [ ] | |
A. |
+1 |
B. |
+2 |
C. |
+3 |
D. |
-1 |
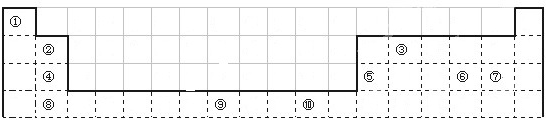
下表列出了某短周期元素R的各级电离能数据(用I1、I2…表示,单位为kJ?mol-1).
|
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com