
题目列表(包括答案和解析)
CH3COOH![]() CH3COO-+H+(电离平衡)
CH3COO-+H+(电离平衡)
Ca(OH)2(s) ![]() Ca2++2OH-(溶解平衡)
Ca2++2OH-(溶解平衡)
*Fe3++SCN-![]() [Fe(SCN)]2+(络合平衡)等
[Fe(SCN)]2+(络合平衡)等
难溶于水的盐在水中存在溶解平衡,其饱和溶液(达到溶解平衡时的溶液)中各离子的浓度遵循一定的定量关系。例如AgCl在水中存在平衡:AgCl![]() Ag++Cl-,在一定温度下,饱和溶液中Ag+的物质的量浓度和Cl-的物质的量浓度的乘积为一常数,可用Ksp表示,Ksp=c(Ag+)·c(Cl-)。已知碳酸钙和氢氧化钙在水中存在下列溶解平衡:Ca(OH)2(s)
Ag++Cl-,在一定温度下,饱和溶液中Ag+的物质的量浓度和Cl-的物质的量浓度的乘积为一常数,可用Ksp表示,Ksp=c(Ag+)·c(Cl-)。已知碳酸钙和氢氧化钙在水中存在下列溶解平衡:Ca(OH)2(s)![]() Ca2++2OH-,CaCO3(s)
Ca2++2OH-,CaCO3(s)![]() Ca2++CO
Ca2++CO![]() 。在火力发电厂燃烧煤的废气中往往含有SO2、O2、N2、CO2等。为了除去有害气体SO2并变废为宝,常常用粉末状的碳酸钙或熟石灰的悬浊液洗涤废气,反应产物为石膏。
。在火力发电厂燃烧煤的废气中往往含有SO2、O2、N2、CO2等。为了除去有害气体SO2并变废为宝,常常用粉末状的碳酸钙或熟石灰的悬浊液洗涤废气,反应产物为石膏。
思考:(1)写出上述两个反应的化学方程式。
(2)试说明用熟石灰的悬浊液而不用澄清石灰水的理由。
已知AgCl为难溶于水和酸的白色固体,Ag2S为难溶于水和酸的黑色固体。向AgCl和水的悬浊液中加入足量的Na2S溶液并振荡,结果白色固体完全转化为黑色固体:
(1)写出白色固体转化为黑色固体的离子方程式:__________________________。
(2)简要说明白色固体转化为黑色固体的原因:____________________________。
(3)已知难溶于水的盐在水中存在溶解平衡,氯化银在水中的溶解平衡为:
AgCl(s) Ag++ Cl-
一定温度下,水溶液中银离子(Ag+)和氯离子(Cl-)的物质的量浓度的乘积为一常数,可用Ksp表示:Ksp=c(Ag+)•c(Cl-)=1.8×10-10
现把氯化银(足量)分别放入:① 100 mL蒸馏水中;② 100 mL 0.1 mol•L-1盐酸溶液中;③ 1 000 mL 0.1 mol•L-1的氯化铝溶液中;④ 100 mL 0.01 mol•L-1的氯化镁溶液中,充分搅拌后,相同温度下,银离子浓度由大到小的顺序是___________(用序号回答)。在0.1mol•L-1氯化铝溶液中,银离子的物质的量浓度最大可达到___________mol•L-1。
已知AgCl为难溶于水和酸的白色固体,Ag2S为难溶于水和酸的黑色固体。向AgCl和水的悬浊液中加入足量的Na2S溶液并振荡,结果白色固体完全转化为黑色固体:
(1)写出白色固体转化为黑色固体的离子方程式:__________________________。
(2)简要说明白色固体转化为黑色固体的原因:____________________________。
(3)已知难溶于水的盐在水中存在溶解平衡,氯化银在水中的溶解平衡为:
AgCl(s) Ag+ + Cl-
Ag+ + Cl-
一定温度下,水溶液中银离子(Ag+)和氯离子(Cl-)的物质的量浓度的乘积为一常数,可用Ksp表示:Ksp=c(Ag+)?c(Cl-)=1.8×10-10
现把氯化银(足量)分别放入:① 100 mL蒸馏水中;② 100 mL 0.1 mol?L-1盐酸溶液中;③ 1 000 mL 0.1 mol?L-1的氯化铝溶液中;④ 100 mL 0.01 mol?L-1的氯化镁溶液中,充分搅拌后,相同温度下,银离子浓度由大到小的顺序是___________(用序号回答)。在0.1 mol?L-1氯化铝溶液中,银离子的物质的量浓度最大可达到___________mol?L-1。
已知AgCl为难溶于水和酸的白色固体,Ag2S为难溶于水和酸的黑色固体。向AgCl和水的悬浊液中加入足量的Na2S溶液并振荡,结果白色固体完全转化为黑色固体:
(1)写出白色固体转化为黑色固体的离子方程式:__________________________。
(2)简要说明白色固体转化为黑色固体的原因:____________________________。
(3)已知难溶于水的盐在水中存在溶解平衡,氯化银在水中的溶解平衡为:
AgCl(s) 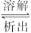 Ag+
+ Cl-
Ag+
+ Cl-
一定温度下,水溶液中银离子(Ag+)和氯离子(Cl-)的物质的量浓度的乘积为一常数,可用Ksp表示:Ksp=c(Ag+)•c(Cl-)=1.8×10-10
现把氯化银(足量)分别放入:① 100 mL蒸馏水中;② 100 mL 0.1 mol•L-1盐酸溶液中;③ 1 000 mL 0.1 mol•L-1的氯化铝溶液中;④ 100 mL 0.01 mol•L-1的氯化镁溶液中,充分搅拌后,相同温度下,银离子浓度由大到小的顺序是___________(用序号回答)。在0.1 mol•L-1氯化铝溶液中,银离子的物质的量浓度最大可达到___________mol•L-1。
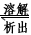 Ag+ + Cl- 一定温度下,水溶液中银离子(Ag+)和氯离子(Cl-)的物质的量浓度的乘积为一常数,可用Ksp表示:Ksp=c(Ag+)·c(Cl-)=1.8×10-10 现把氯化银(足量)分别放入:
Ag+ + Cl- 一定温度下,水溶液中银离子(Ag+)和氯离子(Cl-)的物质的量浓度的乘积为一常数,可用Ksp表示:Ksp=c(Ag+)·c(Cl-)=1.8×10-10 现把氯化银(足量)分别放入:湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com